题目内容
5.氢气还原氧化亚铁:FeO+H2$\frac{\underline{\;\;△\;\;}}{\;}$ H2O+Fe,在该反应中( )| A. | Fe做还原剂 | B. | FeO做氧化剂 | ||
| C. | 铁元素的化合价降低 | D. | 铁元素化合剂升高 |
分析 FeO+H2$\frac{\underline{\;\;△\;\;}}{\;}$ H2O+Fe中,铁元素的化合价降低,H元素的化合价升高,以此来解答.
解答 解:A、Fe是还原产物,故A错误;
B、氧化亚铁中铁元素化合价降低是氧化剂,故B正确;
C、氧化亚铁中铁元素化合价由+2价到0价,故C正确;
D、氧化亚铁中铁元素化合价降低,故D错误;
故选BC.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意基本概念的分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.能正确表示下列化学反应的离子方程式的是( )
| A. | 氢氧化铜与盐酸的反应 Cu(OH)2+2H+=Cu2++2 H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag | |
| D. | 碳酸钙溶于盐酸中 CaCO3+H+=Ca2++H2O+CO2↑ |
17.下列反应通过一步反应不能实现的是( )
| A. | CuO→Cu(OH)2 | B. | CaCO3→CaCl2 | C. | Na2SO4→NaCl | D. | Mg(NO3)2→KNO3 |
14.已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如图:
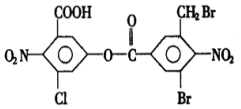
1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑醇羟基和硝基与氢氧化钠的反应,下同),溶液蒸干得到的固体产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为b,则a,b分别是( )
已知:RCH2COONa+NaOH(CaO)$\stackrel{△}{→}$RCH3+Na2CO3.

1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑醇羟基和硝基与氢氧化钠的反应,下同),溶液蒸干得到的固体产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为b,则a,b分别是( )
已知:RCH2COONa+NaOH(CaO)$\stackrel{△}{→}$RCH3+Na2CO3.
| A. | 5mol,10mol | B. | 6mol,2mol | C. | 8mol,4mol | D. | 8mol,2mol |
15.下列各组离子在溶液中能大量共存的是( )
| A. | Na+、Mg2+、Cl-、SO42- | B. | Cu2+、Cl-、NO3-、OH- | ||
| C. | Ca2+、Na+、CO32-、NO3- | D. | K+、Fe3+、NO3-、SCN- |