题目内容
14.下列说法中,正确的是( )| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{14}$C原子的中子数相等 | |
| B. | 纯水在20℃比在90℃时的pH值小 | |
| C. | 正常雨水PH等于7,酸雨的PH小于7 | |
| D. | 次氯酸是一种强氧化剂,是一种弱酸 |
分析 A、根据质量数-质子数=中子数来计算;
B、温度升高促进水的电离,水的离子积常数增大;
C、pH<5.6的雨水称为酸雨;
D、次氯酸属于弱酸,具有氧化性.
解答 解:A、${\;}_{6}^{12}$C和${\;}_{6}^{14}$C原子的中子数分别是6、8,不相等,故A错误;
B、温度升高促进水的电离,纯水中氢离子浓度在20℃比在90℃时的小,即纯水在20℃比在90℃时的pH值大,故B错误;
C、酸雨的PH小于5.6,故C错误;
D、次氯酸属于一元弱酸,其中的Cl显示+1价,次氯酸具有氧化性,故D正确.
故选D.
点评 本题涉及水电离程度和温度关系、酸雨的pH、种子数和质量数以及质子数的关系知识,属于综合知识的考查,难度中等.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
4.某气体的摩尔质量为Mg/mol NA表示阿伏伽德罗常数的值,在一定温度和压强下,体积为VL的该气体所含的分子数为x,MX/VNA表示的是( )
| A. | 以为单位1L 该气体的质量 | B. | 以“克”为单位,VL该气体的质量 | ||
| C. | 1L该气体中所含的分子数 | D. | 以“升”为单位 1mol该气体的体积 |
2.结构简式为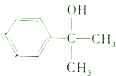 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
9.取PH均等于2的盐酸和醋酸分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A. | 醋酸和锌反应放出的氢气多 | |
| B. | 盐酸和醋酸分别与锌反应放出的氢气一样多 | |
| C. | 醋酸和锌反应速率较大 | |
| D. | 盐酸和醋酸分别与锌反应速率一样大 |
19.下列关于元素周期表的说法中,正确的是( )
| A. | 元素周期表有 18 个族 | |
| B. | 1-20 号元素称为短周期元素 | |
| C. | 元素周期表中有 7 个主族,7 个副族 | |
| D. | 零族元素原子最外层均为 8 个电子 |
6.下列反应属于吸热反应的是( )
| A. | 盐酸与氢氧化钠溶液的反应 | B. | 生石灰和水的反应 | ||
| C. | 氢气在高温下与氧化铜的反应 | D. | 木炭在氧气中燃烧 |
4.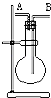 某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2.下列说法正确的是( )
某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2.下列说法正确的是( )
 某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2.下列说法正确的是( )
某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2.下列说法正确的是( )| A. | 烧瓶是干燥的,由B进气,可收集②③④⑥⑦ | |
| B. | 烧瓶是干燥的,由A进气,可收集①⑤ | |
| C. | 在烧瓶中充满水,由A进气,可收集①⑤⑦ | |
| D. | 在烧瓶中充满水,由B进气,可收集⑥ |