题目内容
下列各组实验中溶液最先变浑浊的是( )
| A、0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B、0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C、0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度60℃ |
| D、0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:表中给出的数据为浓度和温度的影响,一般来说,浓度越大,温度越高,反应速率越大,以此解答该题.
解答:
解:对于该反应来说浓度越大,温度越高,反应速率越大,表中C温度较高,且浓度最大,则应大于A、B、D的反应速率,
故选C.
故选C.
点评:本题考查化学反应速率,为高考高频考点,侧重于反应速率的影响因素的考查以及数据处理能力,能较好的培养学生良好的科学素养,难度不大,学习中注意掌握影响化学反应速率的因素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
气体A、B通式分别为CnH2n+2和CnH2n-2,若用催化剂使250mL混合气体加氢,在相同条件下需要H2 100mL,则原混合气体中A、B两体积之比为( )
| A、1:2 | B、1:3 |
| C、1:4 | D、4:1 |
0.1mol某有机物的蒸气跟足量的O2混合后点燃,反应后生成13.2g CO2和5.4gH2O,该有机物能跟Na反应放出H2,又能跟新制Cu(OH)2反应生成红色沉淀,此有机物还可与乙酸反应生成酯类化合物,该酯类化合物的结构简式可能是( )
| A、OHCCH2CH2COOCH3 |
B、 |
C、 |
D、 |
与标准状况下V L CO2所含有氧原子数目相同的水的质量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
已知298K时,2SO2(g)+O2(g)?2SO3(g)△H=-197kJ?mol-1.在同一温度和压强下,向某密闭容器中通入2mol SO4和1mol O2达到平衡时,反应放出的热量为Q1,向另一相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2.下列关系正确的是( )
A、Q2=
| ||
B、Q2<
| ||
| C、Q2<Q1<197 kJ | ||
| D、Q1=Q2=197 kJ |
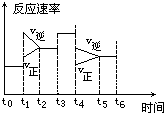 一密封体系中发生下列反应:N2+3H2 2NH3+Q,下图是某一时间段中反应速率与反应进程的曲线关系图:
一密封体系中发生下列反应:N2+3H2 2NH3+Q,下图是某一时间段中反应速率与反应进程的曲线关系图: 放出,如图中符合这一情况的是( )
放出,如图中符合这一情况的是( )