题目内容
如图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体 放出,如图中符合这一情况的是( )
放出,如图中符合这一情况的是( )
 放出,如图中符合这一情况的是( )
放出,如图中符合这一情况的是( )| A极板 | B极板 | X电极 | Z溶液 | |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
| A、A | B、B | C、C | D、D |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:通电后,发现a极板质量增加,b极板处有无色无臭气体放出,则a为阴极,金属阳离子在阴极放电,b为阳极,OH-离子放电生成氧气,电极材料中的阳极一定为惰性电极,阴极材料不确定,以此来解答.
解答:
解:X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色、无臭气体放出,说明a为阴极、b为阳极,溶液中的阳离子氧化性大于氢离子,阳极上生成氧气说明氢氧根离子放电,X为负极,
A.以惰性电极材料为电极时电解硫酸铜溶液,a电极上生成铜、b电极上生成氧气,符合条件,故A正确;
B.以石墨为电极电解氢氧化钠溶液时,a电极上生成氢气而不是金属,不符合条件,故B错误;
C.X为负极而不是正极,故C错误;
D..以惰性电极材料为电极时电解溶液时,X为负极,阳极上氯离子放电生成黄绿色气体,不符合条件,故D错误;
故选A.
A.以惰性电极材料为电极时电解硫酸铜溶液,a电极上生成铜、b电极上生成氧气,符合条件,故A正确;
B.以石墨为电极电解氢氧化钠溶液时,a电极上生成氢气而不是金属,不符合条件,故B错误;
C.X为负极而不是正极,故C错误;
D..以惰性电极材料为电极时电解溶液时,X为负极,阳极上氯离子放电生成黄绿色气体,不符合条件,故D错误;
故选A.
点评:本题考查电解原理,注意信息的获取及利用,结合溶液中离子放电顺序分析发生的电极反应,题目难度中等,氯气为黄绿色气体易被学生忽略.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
将3.5g Fe、Mg合金投入到一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体V L(HNO3被还原为NO和NO2);若向反应后的溶液中加入足量的氢氧化钠溶液,待金属元素全部沉淀后,再将沉淀过滤、洗净、干燥后称量质量为8.6g.则收集到的气体体积V值可能为( )
| A、1.12 | B、5.34 |
| C、7.26 | D、8.23 |
下列各组实验中溶液最先变浑浊的是( )
| A、0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B、0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C、0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度60℃ |
| D、0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
下列有关说法正确的是( )
| A、某反应2A (g)+B(g)═3C(s)在室温下可自发进行,则该反应的△H<0 | ||
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | ||
C、CH3COOH 溶液加水稀释后,溶液中
| ||
| D、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH 减小 |
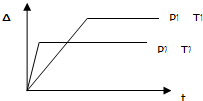 有一化学平衡:mA(气)+nB(气)?pC(气)+qD(气),如图表示A的
有一化学平衡:mA(气)+nB(气)?pC(气)+qD(气),如图表示A的转化率同温度、压强的关系,分析此图可以得出的正确结论是( )
| A、正反应是吸热反应,m+n>p+q |
| B、正反应是吸热反应,m+n<p+q |
| C、正反应是放热反应,m+n>p+q |
| D、正反应是放热反应,m+n<p+q |
下列说法正确的是( )
| A、苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
| B、元素分析仪可以同时对碳、氢、氧、硫等多种元素进行分析 |
| C、乙醇、乙酸均能与金属钠反应产生氢气,是因为它们所含的官能团相同 |
| D、糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同 |
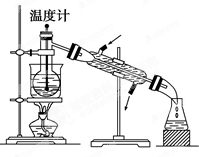 海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图:
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图: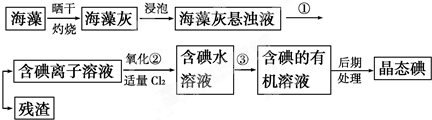
 氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答: