题目内容
13.实验室配制500mL 0.2mol/L的Na2SO4溶液,实验操作步骤有:A.在天平上称取一定质量的硫酸钠固体,把它放在烧杯中,用适量的蒸馏水使它完全溶解并冷却至室温.
B.把制得的溶液小心地转移到容量瓶中.
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低处与刻度线相切.
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心注入容量瓶并轻轻振荡.
E.将容量瓶瓶塞塞紧,充分摇匀.
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)ABDCE.
(2)操作A中,在天平上称取硫酸钠固体的质量为14.2g.
(3)本实验用到的基本仪器已经有烧杯、天平(带砝码、镊子)、玻璃棒,还缺少的仪器是500mL容量瓶、胶头滴管、药匙.
(4)①在配制溶液过程中,若缺少操作D,将使配制的溶液浓度偏低(填“偏高”或“偏低”或“无影响”).②操作C中加蒸馏水时,不慎超过了刻度线,将使配制的溶液浓度偏低(填“偏高”或“偏低”或“无影响”).
(5)下列操作中,容量瓶所不具备的功能有BCE.
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质.
分析 (1)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶贴标签,据此排序;
(2)依据m=CVM计算需要溶质的质量;
(3)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
(5)容量瓶不能稀释浓溶液、不能用于溶解固体、储存溶液,不能用来测量容量瓶规格以下的任意体积的液体,是用来配制一定体积、一定物质的量浓度溶液的专用仪器等;
解答 解:(1)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶贴标签,所以正确的顺序为:ABDCE;
故答案为:ABDCE;
(2)配制500mL 0.2mol/L的Na2SO4溶液,需要溶质的质量m=0.5L×0.2mol/L×142g/mol=14.2g;
故答案为:14.2;
(3)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶贴标签,用到的仪器:托盘天平、钥匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以还缺少的仪器:500mL容量瓶、胶头滴管、药匙;
故答案为:500mL容量瓶、胶头滴管、药匙;
(4))①在配制溶液过程中,若缺少操作D,导致部分溶质损耗,溶质的物质的量偏小,将使配制的溶液浓度偏低;
故答案为:偏低;
②操作C中加蒸馏水时,不慎超过了刻度线,导致溶液体积偏大,将使配制的溶液浓度偏低;
故答案为:偏低;
(5)容量瓶只能用来配制一定体积准确浓度的溶液,不能配制或测量容量瓶规格以下的任意体积的液体,不能稀释或溶解药品,不能用来加热溶解固体溶质,
故选:BCE;
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶的使用方法和注意问题,注意误差分析的方法,题目难度不大.

 在密闭容器中进行下列反应:M (g)+N (g)?R (g)+2L.此反应符合右面图象,下列有关叙述正确的是( )
在密闭容器中进行下列反应:M (g)+N (g)?R (g)+2L.此反应符合右面图象,下列有关叙述正确的是( )| A. | 正反应放热,L是气体 | B. | 正反应吸热,L是气体 | ||
| C. | 正反应放热,L不是气体 | D. | 正反应吸热,L不是气体 |
 如图:A处通入氯气,关闭B阀时,C处干燥红色布条无变化,打开B阀时,C处干燥的红色布条褪色.则下列说法正确的是( )
如图:A处通入氯气,关闭B阀时,C处干燥红色布条无变化,打开B阀时,C处干燥的红色布条褪色.则下列说法正确的是( )| A. | D中可以盛放浓硫酸 | B. | D中可以盛放饱和食盐水 | ||
| C. | D中可以盛放水 | D. | A处通入的是干燥的氯气 |
| A. | pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)>c(CH3COO-) | |
| B. | 强电解质溶液的导电性一定比弱电解质溶液的导电性强 | |
| C. | AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同 | |
| D. | pH=4.0的番茄汁中c(H+)是pH=6.0的牛奶中c(H+)的100倍 |
| A. | 依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等 | |
| B. | 依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 依据分散质粒子直径的大小,将分散系分为溶液、胶体、浊液 | |
| D. | 依据组成元素的种类,将纯净物分为单质和化合物 |
| A. | Na2O | B. | CaCO3 | C. | Ca(OH)2 | D. | C2H12O6 |
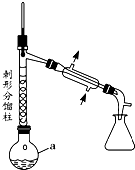 乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下: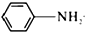 +CH3COOH$\stackrel{△}{?}$
+CH3COOH$\stackrel{△}{?}$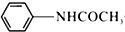 +H2O
+H2O已知:
①苯胺易被氧化.
②乙酰苯胺、苯胺和醋酸的部分物理性质如下表:
| 物质 | 熔点 | 沸点 | 溶解度 |
| 乙酰苯胺 | 114.3℃ | 305℃ | 微溶于冷水、易溶于热水 |
| 苯胺 | -6℃ | 184.4℃ | 微溶于水 |
| 醋酸 | 16.6℃ | 118℃ | 易溶于水 |
步骤1:在a中,加入9mL(0.10mol)苯胺、15mL(0.27mol)冰醋酸及少许锌粉,依照上图装置组装仪器.
步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全.
步骤3:趁热将反应混合物倒入盛有100mL 冷水的烧杯中,冷却后抽滤(一种快速过滤方法)、洗涤,得到粗产品.
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g.
请回答下列问题:
(1)仪器a的名称为圆底烧瓶,所选仪器a的最佳规格是B(填序号).
A.25mL B.50mL C.100mL D.250mL
(2)实验中加入少许锌粉的目的是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中,控制温度计读数在105℃左右的原因是温度过低不能蒸出反应所生成的水或温度过高未反应的乙酸蒸出.
(4)判断反应已基本完全的方法为锥形瓶不再有水增加.
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是若让反应混合物冷却,则固体析出沾在瓶壁上不易处理.
(6)步骤4中粗产品进一步提纯,该提纯方法是重结晶.
(7)本次实验的产率为80%.
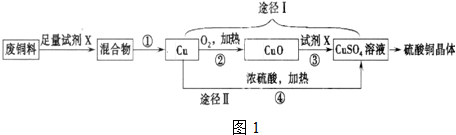

 在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.