题目内容
20.含FeS265%的硫铁矿在煅烧时有1.8%的硫损失而混入炉渣,二氧化硫转化为三氧化硫的利用率为99%.由这种硫铁矿制2t98%的硫酸,需硫铁矿多少吨?分析 根据反应的转化关系式计算,关系式为:FeS2~2SO2~2SO3~2H2SO4.
解答 解:设需这种硫铁矿的质量为x.
FeS2 ~2SO2 ~2SO3 ~2H2SO4
120 2×98
x×65%×(1-1.8%)×99% 2t×98%
$\frac{120}{x×65%×(1-1.8%)×99%}=\frac{2×98}{2t×98%}$
解之得:x=189.9t
答:需硫铁矿189.9吨.
点评 本题考查化学方程式的计算,题目难度中等,注意关系式法的利用,要注意运用某一种化合物中元素的损失率=该化合物的损失率,另外,耗损和利用率、产率和纯度的关系要处理正确,关系式多用于工业生产中的计算题.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
10.向50mL 1mol/L AlCl3溶液中加入1.5mol/L NaOH溶液amL,充分反应后,生成白色沉淀1.56g,则a的数值可能是( )
| A. | 40和120 | B. | 65和90 | C. | 40和90 | D. | 90和120 |
11.下列物质中含有共价键的离子化合物是( )
| A. | CaF2 | B. | KOH | C. | CO2 | D. | CH4 |
8.图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中第一电离能最小的是B(填编号).比元素B原子序数大10的元素在元素周期表中的位置:三周期,ⅠB族,其基态原子的核外电子排布是1s22s22P63s23P63d104s1.
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是CO2、PCl3或CCl4(写分子式,写出两种即可),元素G、I分别和J形成的两种化合物的晶体类型是分子晶体、原子晶体.
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成7个σ键,1个π键.
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第ⅢA族.

图(B)是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第ⅣA族元素氢化物的沸点的变化规律.
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是b_.
| 性质 元素 | A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中第一电离能最小的是B(填编号).比元素B原子序数大10的元素在元素周期表中的位置:三周期,ⅠB族,其基态原子的核外电子排布是1s22s22P63s23P63d104s1.
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是CO2、PCl3或CCl4(写分子式,写出两种即可),元素G、I分别和J形成的两种化合物的晶体类型是分子晶体、原子晶体.
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成7个σ键,1个π键.
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第ⅢA族.

图(B)是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第ⅣA族元素氢化物的沸点的变化规律.
不同同学对某主族元素的氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是b_.
15. 随着原子序数的递增,五种短周期元素原子半径的相对大小和最高正价或最低负价如图所示.下列说法不正确的是( )
随着原子序数的递增,五种短周期元素原子半径的相对大小和最高正价或最低负价如图所示.下列说法不正确的是( )
 随着原子序数的递增,五种短周期元素原子半径的相对大小和最高正价或最低负价如图所示.下列说法不正确的是( )
随着原子序数的递增,五种短周期元素原子半径的相对大小和最高正价或最低负价如图所示.下列说法不正确的是( )| A. | X2W能与WY2反应生成W | |
| B. | 气态氢化物的稳定性:W>Q | |
| C. | Y分别与其它四种元素均可形成至少两种以上化合物 | |
| D. | Y、Z、Q三种元素组成化合物的水溶液可能呈中性,也可能呈碱性 |
12.目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确是( )
| A. | 碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键 | |
| B. | 碳原子性质活泼,可以跟多数元素原子形成共价键 | |
| C. | 碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键 | |
| D. | 很多含碳的物质存在同分异构体 |
10.下列离子方程式书写正确的是( )
| A. | 钠投入水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2 | |
| C. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+═2H2O+I2 |
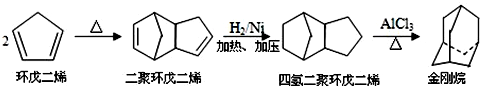
 其中,反应③的反应类型是加成反应.
其中,反应③的反应类型是加成反应.