题目内容
9.金刚烷是一种重要的化工原料,工业上可通过下列途径制备: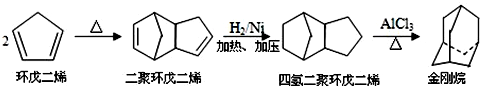
请回答下列问题:
(1)环戊二烯分子中最多有9个原子共平面;
(2)金刚烷的分子式为C10H16,其分子中的CH2基团有6个;其一氯取代物有2种.
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
 其中,反应③的反应类型是加成反应.
其中,反应③的反应类型是加成反应.
分析 (1)由碳碳双键为平面结构分析环戊二烯分子中最多共平面的原子数;
(2)金刚烷的分子中有6个CH2,4个CH结构,据此判断其分子式;根据分子中氢原子的种类等于一氯取代物的种类;
(3)由合成路线可知,反应①为光照条件下的取代反应,反应②为消去反应,反应③为加成反应,反应④为消去反应,以此来解答.
解答 解:(1)C=C为平面结构,与双键碳直接相连的原子一定在同一平面内,则5个C和4个H在同一平面内,
故答案为:9;
(2)由C原子形成4个共价键,由结构简式可知金刚烷的分子中有6个CH2,4个CH结构,分子式为C10H16,分子中含2种位置的H,则一氯代物有2种;
故答案为:C10H16;6;2;
(3)由合成路线可知,反应①为光照条件下的取代反应,其产物名称为氯代环戊烷;反应②卤素原子的消去反应,反应条件为氢氧化钠的醇溶液;反应③为加成反应,反应④为卤代烃的消去反应.
故答案为:加成反应.
点评 本题考查有机物的合成,题目难度中等,注意把握有机物的官能团、碳链骨架等的变化,明确发生的反应及习题中的信息即可解答,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
19.X、Y、Z均为短周期元素,它们的原子核外最外层电子数分别为1、6、6,Z位于Y的上一周期,则这三种元素形成的某种化合物的化学式可能为( )
| A. | X2YZ4 | B. | XY2Z3 | C. | X3YZ4 | D. | XYZ3 |
17.铁铝合金是一种新型高温结构材料,取一定量的铁铝合金完全溶于盐酸中,然后通入过量的氯气,再加入过量的烧碱溶液,溶液中能够存在较多的阳离子为( )
| A. | Na+、Fe3+、Al3+、H+ | B. | Na+ | ||
| C. | Na+、Fe3+ | D. | Na+、Fe2+、Al3+ |
4.常温、常压下,50ml三种气态烃的混合物与足量的氧气混合后点燃爆炸,恢复到原来状况时,体积共缩小100ml,则三种烃可能是( )
| A. | CH4、C2H6、C3H4 | B. | C2H6、C3H6、C4H6 | C. | CH4、C2H6、C3H8 | D. | C2H4、C2H6、C2H2 |
14.关于如图中四个图象的说法正确的是( )

注:图中,E表示能量,p表示压强,t表示时间,V表示体积.

注:图中,E表示能量,p表示压强,t表示时间,V表示体积.
| A. | ①表示化学反应H2(g)+Cl2(g)═2HCl(g)的能量变化,则该反应的反应热△H=+183 kJ/mol | |
| B. | ②表示其他条件不变时,反应4A(g)+3B(g)?2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是气体 | |
| C. | ③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | ④表示10 mL 0.1 mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1 mol/L盐酸,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
1.将1.92g Cu投入到一定量的浓HNO3中,Cu完全溶解,共收集到标准状况下672mL NO和NO2的混合气体.将盛有此气体的容器倒扣在水槽中,并通入一定体积的O2,恰好使水充满整个容器.则通入的O2的体积在标准状况下为( )
| A. | 168 mL | B. | 224 mL | C. | 336 mL | D. | 504 mL |
18.下列物质可用来除去乙烷中的乙烯气体的是( )
| A. | 浓H2SO4 | B. | NaOH | C. | Br2的CCl4溶液 | D. | 酸性KMnO4溶液 |
19.21世纪进入信息时代,两位美国化学家和一位日本化学家在导电塑料领域功勋卓著,他们首先把聚乙炔树脂制成导电塑料,开创塑料导电的新纪元.下列关于聚乙炔的叙述错误的是 ( )
| A. | 聚乙炔是以乙炔为单体发生加聚反应形成的高聚物 | |
| B. | 聚乙炔的化学式为 ,其分子中所有碳原子不可能在同一直线上 ,其分子中所有碳原子不可能在同一直线上 | |
| C. | 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质 | |
| D. | 1摩尔聚乙炔能与1摩尔Br2发生加成反应 |