题目内容
19.氮化硅是新型无机非金属材料,其中Si与N原子最外层均达到8电子结构.下列关于它的说法不正确的是( )| A. | 硅与氮的原子数之比为4:3 | |
| B. | 氮原子与硅原子间以共价键相结合 | |
| C. | 熔点高,硬度大,可用于制造柴油机 | |
| D. | amol氮化硅含有质子数的物质的量为70amol |
分析 A.氮化硅为立体网状结构,每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连;
B.非金属元素之间存在共价键;
C.根据原子晶体的性质分析;
D.根据氮化硅的化学式分析.
解答 解:A.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连,晶体的化学式为Si3N4,故A错误;
B.氮原子与硅原子都为非金属元素,氮原子与硅原子间以共价键相结合,故B正确;
C.氮化硅是新型无机非金属材料,是超硬新材料,属于原子晶体的典型物理性质,可用于制造柴油机,故C正确;
D.1个硅原子含有14个质子,1个氮原子含有7个质子,氮化硅的化学式为Si3N4,amol氮化硅含有质子数的物质的量为70amol,故D正确;
故选A.
点评 本题考查了原子晶体的化学键与性质,注意氮化硅为原子晶体每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连为解答关键,题目难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
7.NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 16g由O2和O3的混合气体中含有的分子数为0.5NA | |
| B. | 2.3g金属钠在装有氧气的集气瓶中完全燃烧,转移的电子数为0.1NA | |
| C. | 100mL 12mol/L浓盐酸与足量MnO2共热,生成的Cl2分子数为0.3NA | |
| D. | 0.3molAgNO3受热完全分解(2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑ ),用排水收集到气体的分子数为0.25NA |
14.下列离子方程式书写正确的是( )
| A. | Na2SO3溶液中加入稀硝酸:SO32-+2H+═SO2↑+H2O | |
| B. | NH4HSO3溶液与少量的NaOH溶液混合加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O | |
| C. | FeBr2溶液中通入足量的Cl2:4Fe2++4Br-+3Cl2═4Fe3++2Br2+6Cl- | |
| D. | 向碳酸氢钙溶液加入少量氢氧化钾溶液:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- |
4.加热蒸干以下物质的溶液,不能析出原溶质固体的是( )
| A. | Fe2(SO4)3 | B. | FeCl3 | C. | Na2CO3 | D. | KCl |
11.如图所示装置是“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中是否有CO2和CO.(图中夹持装置及尾气处理装置均已略去)
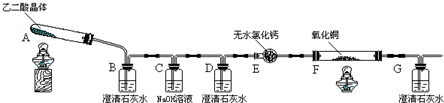
(1)装置C中盛放NaOH溶液的作用是吸收乙二酸晶体受热分解生成的二氧化碳.
(2)①证明分解产物中有CO2的现象是装置B中澄清石灰水变浑浊.
②证明分解产物中有CO的现象是装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊.
(3)实验结束后,装置F中黑色氧化铜变为红色固体.简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):取少量红色固体,滴加稀硫酸,观察红色固体是否有部分溶解,溶液是否变蓝色.
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4氧化生成CO2.KMnO4和草酸钠在稀硫酸中反应的离子方程式是:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O.
②实验室常用草酸钠标定KMnO4溶液.操作如下:准确称取0.2000g草酸钠,放入锥形瓶中,加100mL稀硫酸溶解,用配置好的KMnO4溶液滴定.当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30s不褪色,即达到滴定终点.重复上述滴定操作三次,实验数据如下表所示.
KMnO4溶液的物质的量浓度的计算式是c(KMnO4)=$\frac{0.2000g×2mol}{5mol×134g/mol×0.01601L}$.

(1)装置C中盛放NaOH溶液的作用是吸收乙二酸晶体受热分解生成的二氧化碳.
(2)①证明分解产物中有CO2的现象是装置B中澄清石灰水变浑浊.
②证明分解产物中有CO的现象是装置D中澄清石灰水不变浑浊,装置F中黑色氧化铜变为红色固体,装置G中澄清石灰水变浑浊.
(3)实验结束后,装置F中黑色氧化铜变为红色固体.简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):取少量红色固体,滴加稀硫酸,观察红色固体是否有部分溶解,溶液是否变蓝色.
(4)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4氧化生成CO2.KMnO4和草酸钠在稀硫酸中反应的离子方程式是:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O.
②实验室常用草酸钠标定KMnO4溶液.操作如下:准确称取0.2000g草酸钠,放入锥形瓶中,加100mL稀硫酸溶解,用配置好的KMnO4溶液滴定.当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30s不褪色,即达到滴定终点.重复上述滴定操作三次,实验数据如下表所示.
| 滴定前 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管 液面刻度 | 0.00mL | 16.02mL | 16.00mL | 16.01mL |
 合理选择饮食,有益身体健康.小明家某次晚餐菜谱如图所示.
合理选择饮食,有益身体健康.小明家某次晚餐菜谱如图所示.
 短周期元素A、B、C的位置如图所示:已知B、C两元素的原子序数之和是A元素的4倍,则C为氯(填元素名称).
短周期元素A、B、C的位置如图所示:已知B、C两元素的原子序数之和是A元素的4倍,则C为氯(填元素名称).