题目内容
根据下列框图回答问题:

已知:化合物A的组成中含有六个结晶水,A、B均溶于水,G是一种重要化工原料.(图中部分反应物或生成物已略去).
(1)写出晶体A的化学式:______; 物质B的电子式:______.
(2)写出C→D+E反应的化学方程式:______.
(3)写出气体I通入H的溶液中反应的离子方程式:______;
(4)某同学取H的溶液,通入气体D,所得溶液中仍只有一种阴离子.请写出上述变化过程中的离子方程式:______.
解:由转化关系可知,白色沉淀L不溶于盐酸,L为BaSO4,滤液2中焰色为紫色,则含K+,红褐色沉淀为Fe(OH)3,则气体I为氨气,H中含Fe3+,由C→D及D→F的转化可知,黑色沉淀C为FeS2,D为SO2,E为Fe2O3,F为SO3,G为硫酸,所以H为硫酸铁,由原子守恒可知,滤液1中含硫酸根离子,化合物A的组成中含有六个结晶水,A、B均溶于水,则A为(NH4)2Fe(SO4)2?6H2O,B为K2S,
(1)由上述分析可知A为(NH4)2Fe(SO4)2?6H2O,B为K2S,其电子式为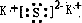 ,故答案为:(NH4)2Fe(SO4)2?6H2O;
,故答案为:(NH4)2Fe(SO4)2?6H2O;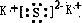 ;
;
(2)C→D+E反应的化学方程式为4FeS+7O2 2Fe2O3+4SO2,故答案为:4FeS+7O2
2Fe2O3+4SO2,故答案为:4FeS+7O2 2Fe2O3+4SO2;
2Fe2O3+4SO2;
(3)I通入H的溶液中反应的离子方程式为Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,故答案为:Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
(4)H的溶液,通入气体D,所得溶液中仍只有一种阴离子,该离子反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
分析:由转化关系可知,白色沉淀L不溶于盐酸,L为BaSO4,滤液2中焰色为紫色,则含K+,红褐色沉淀为Fe(OH)3,则气体I为氨气,H中含Fe3+,由C→D及D→F的转化可知,黑色沉淀C为FeS2,D为SO2,E为Fe2O3,F为SO3,G为硫酸,所以H为硫酸铁,由原子守恒可知,滤液1中含硫酸根离子,化合物A的组成中含有六个结晶水,A、B均溶于水,则A为(NH4)2Fe(SO4)2?6H2O,B为K2S,然后结合元素化合物知识及化学用语来解答.
点评:本题考查无机物的推断,沉淀的颜色和焰色反应为解答本题的突破口,注意利用元素、原子守恒的方法逆推出各物质,熟悉氧化还原反应即可解答,题目难度中等.
(1)由上述分析可知A为(NH4)2Fe(SO4)2?6H2O,B为K2S,其电子式为
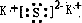 ,故答案为:(NH4)2Fe(SO4)2?6H2O;
,故答案为:(NH4)2Fe(SO4)2?6H2O;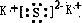 ;
;(2)C→D+E反应的化学方程式为4FeS+7O2
 2Fe2O3+4SO2,故答案为:4FeS+7O2
2Fe2O3+4SO2,故答案为:4FeS+7O2 2Fe2O3+4SO2;
2Fe2O3+4SO2;(3)I通入H的溶液中反应的离子方程式为Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,故答案为:Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
(4)H的溶液,通入气体D,所得溶液中仍只有一种阴离子,该离子反应为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
分析:由转化关系可知,白色沉淀L不溶于盐酸,L为BaSO4,滤液2中焰色为紫色,则含K+,红褐色沉淀为Fe(OH)3,则气体I为氨气,H中含Fe3+,由C→D及D→F的转化可知,黑色沉淀C为FeS2,D为SO2,E为Fe2O3,F为SO3,G为硫酸,所以H为硫酸铁,由原子守恒可知,滤液1中含硫酸根离子,化合物A的组成中含有六个结晶水,A、B均溶于水,则A为(NH4)2Fe(SO4)2?6H2O,B为K2S,然后结合元素化合物知识及化学用语来解答.
点评:本题考查无机物的推断,沉淀的颜色和焰色反应为解答本题的突破口,注意利用元素、原子守恒的方法逆推出各物质,熟悉氧化还原反应即可解答,题目难度中等.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目

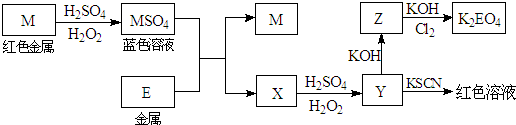
 (2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
(2008?江苏)根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
 .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有