题目内容
5.已知H2S+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$S↓+SO2↑+2H2O.①用双线桥法分析上述反应(只需标出电子得失的方向和数目)
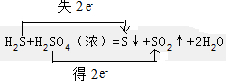 .
.②上述反应中氧化剂是H2SO4(浓),氧化产物是S.若反应中转移了0.6mol电子,产生的气体在标准状况下的体积是6.72L.
分析 H2S+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$S↓+SO2↑+2H2O中,化合价的变化为:H2S→S,S元素由-2价→0价,一个H2S分子失去2个电子,所以H2S是还原剂;S是氧化产物;H2SO4→SO2,S元素由+6价→+4价,一个H2SO4分子得2个电子,该反应中转移电子数为2,以此来解答.
解答 解:①H2S+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$S↓+SO2↑+2H2O中,化合价的变化为:H2S→S,S元素由-2价→0价,还原剂是H2S,一个H2S分子失去2个电子,所以H2S是还原剂;S是氧化产物;H2SO4→SO2,S元素由+6价→+4价,一个H2SO4分子得2个电子,该反应中转移电子数为2,用双线桥标注电子转移方向和数目为: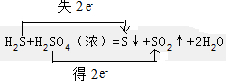 ,故答案为:
,故答案为: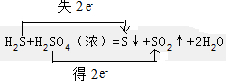 ;
;
②H2S+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$S↓+SO2↑+2H2O中,化合价的变化为:H2S→S,S元素由-2价→0价,还原剂是H2S,S是氧化产物;H2SO4→SO2,S元素由+6价→+4价,则H2SO4(浓)为氧化剂,根据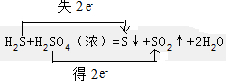 ,若反应中转移了0.6mol电子,产生的气体在标准状况下的体积是$\frac{0.6}{2}$×22.4=6.72L,
,若反应中转移了0.6mol电子,产生的气体在标准状况下的体积是$\frac{0.6}{2}$×22.4=6.72L,
故答案为:H2SO4(浓);S;6.72L.
点评 本题考查氧化还原反应中转移电子数的考查,为高频考点、把握元素的化合价变化、得失电子的方向为解答的关键,注意箭头指向与转移电子总数,题目难度不大.

练习册系列答案
相关题目
13.10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如表变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为HCO3-+H2O?H2CO3+OH-;
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3;
(3)丙同学设计如下实验方案对甲、乙同学的解释进行判断:
将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此可以判断乙(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中有新物质生成.
| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3;
(3)丙同学设计如下实验方案对甲、乙同学的解释进行判断:
将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此可以判断乙(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中有新物质生成.
20.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0;一定温度下,向10L恒容密闭容器中通入N2O5,的部分实验数据见下表:
下列说法不正确的是( )
| t/s | 0 | 500 | 1000 | 1500 |
| n(N2O5)/mol | 5.00 | 3.5 | 2.50 | 2.50 |
| A. | 500s内N2O5分解速率为3×10-4mol•L-1•s-1 | |
| B. | 反应达平衡后,往容器中加入5molN2O5气体,平衡正向移动,反应的热效应不变 | |
| C. | 相同温度下,将体积缩小为原来的$\frac{1}{2}$,达到新平衡时,N2O5(g)的浓度为0.125mol/L | |
| D. | 达到新平衡的压强是初始时的1.75倍 |
17.氢气既是最理想的能源又是重要的化工原料,用甲烷制氢气是一种廉价的制氢方法,有关的热化学方程式如下:
CH4(g)+$\frac{1}{2}$O2(g)?CO(g)+2H2(g)△H<0 ①
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0 ①
下列说法不正确的是( )
CH4(g)+$\frac{1}{2}$O2(g)?CO(g)+2H2(g)△H<0 ①
CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0 ①
下列说法不正确的是( )
| A. | 当反应①中v正(CH4)=v逆(CO)时,表明该反应达平衡状态 | |
| B. | 其他条件不变时,增大体系压强,反应①、②中甲烷的转化率均减小 | |
| C. | 使用高效催化剂可以加快反应速率,同时提高CH4的转化率 | |
| D. | 同一容器内同时发生反应①与②时,容器内温度可能保持不变 |

