题目内容
对下列氧化还原反应中转移电子数的判断,不正确的是( )
| A、H2S+H2SO4(浓)=S↓+SO2↑+2H2O:6e- |
| B、3Cl2+6KOH5KCl+KClO3+3H2O:5e- |
| C、2Na2O2+2H2O=4NaOH+O2↑:2e- |
| D、2H2S+SO2=3S+2H2O:4e- |
考点:氧化还原反应的电子转移数目计算
专题:
分析:根据化合价升高数目=化合价降低数目=转移的电子数目进行判断.
解答:
解:A.硫酸中S的化合价由+6价降低为+4价,降低2,故生成SO2转移电子数为2e-,故A错误;
B.氯气中氯的化合价由0价升高为+5价,升高5,故生成KClO3转移电子数为5e-,故B正确;
C.Na2O2中O的化合价由-1价升高为0价,升高1,故生成O2转移电子数为2e-,故C正确;
D.SO2中硫的化合价由+4价降低为0价,降低4,故生成S转移电子数为4e-,故D正确;
故选A.
B.氯气中氯的化合价由0价升高为+5价,升高5,故生成KClO3转移电子数为5e-,故B正确;
C.Na2O2中O的化合价由-1价升高为0价,升高1,故生成O2转移电子数为2e-,故C正确;
D.SO2中硫的化合价由+4价降低为0价,降低4,故生成S转移电子数为4e-,故D正确;
故选A.
点评:本题考查氧化还原反应中转移电子数的判断,难度不大.要注意化合价升高数目=化合价降低数目=转移的电子数目是解题的关键.

练习册系列答案
相关题目
2006年5月15日,国家食品药品监督管理局通报查处了齐齐哈尔第二制药有限公司使用工业溶剂二甘醇(HO-CH2-CH2-O-CH2-CH2-OH)代替药用溶剂丙二醇(HO-CH2-CH2-CH2-OH)的事件.最新统计,目前确定齐齐哈尔第二制药有限公司生产的“亮菌甲素”假药造成的死亡人数已有9人.下列关于二甘醇说法正确的是( )
| A、二甘醇和丙二醇性质完全相同 |
| B、二甘醇和丙二醇互为同系物 |
| C、二甘醇沸点可能比丙二醇高 |
| D、二甘醇在人体中的降解产物草酸(HOOC-COOH)对人体有害 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、25℃时,2LpH=1的H2SO4溶液中,SO42-数目为0.1NA | ||
| B、300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA | ||
C、标准状况下,V L CHCl3含有的碳原子数为
| ||
| D、1 mol OH-参与电解,反应过程中转移的电子数为NA |
下列反应的离子方程式正确的是( )
| A、铁和稀盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
| B、碳酸钙溶于稀盐酸中 CO32-+2H+=CO2↑+H2O |
| C、碳酸氢钠溶液与盐酸反应 HCO3-+H+=CO2↑+H2O |
| D、氧化铜与盐酸反应 O2-+2H+=H2O |
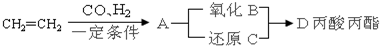
 ,
,