题目内容
16.某同学欲配制480mL物质的量浓度为0.1mol/L的CuSO4溶液.(1)完成该实验用到的仪器主要有:托盘天平、胶头滴管、500mL容量瓶,烧杯、玻璃棒、药匙.
(2)如果用CuSO4固体来配制,应该称量固体的质量为8.0g.
(3)下列操作对溶液的浓度有何影响?用“偏大”“偏小”或“无影响”填空.
①配制的过程中有少量的液体溅出烧杯.偏小
②使用前容量瓶用蒸馏水洗涤,且没有干燥.无影响
③定容时俯视液面.偏大.
分析 配制480mL物质的量浓度为0.1mol/L的CuSO4溶液,选择500mL容量瓶,在结合m=cVM计算质量,然后称量、在烧杯中溶解、冷却后转移到容量瓶中定容,结合c=$\frac{n}{V}$及不当操作对n、V的影响判断误差.
解答 解:(1)配制480mL溶液,需要500mL容量瓶,还需要托盘天平、胶头滴管、烧杯、玻璃棒、药匙,故答案为:500mL容量瓶;
(2)用CuSO4固体来配制,应该称量固体的质量为0.5L×0.1mol/L×160g/mol=8.0g,故答案为:8.0g;
(3)①配制的过程中有少量的液体溅出烧杯,n偏小,由c=$\frac{n}{V}$可知,c偏小,故答案为:偏小;
②使用前容量瓶用蒸馏水洗涤,且没有干燥,对n、V均无影响,则c无影响,故答案为:无影响;
③定容时俯视液面,V偏小,由c=$\frac{n}{V}$可知,c偏大,故答案为:偏大.
点评 本题考查配制一定浓度的溶液,为高频考点,把握配制溶液需要的仪器、步骤、误差分析为解答的关键,侧重分析与实验能力的考查,注意结合浓度公式分析误差,题目难度不大.

练习册系列答案
相关题目
7.下列各反应中,氧化反应与还原反应在同种元素中进行的是( )
| A. | Cl2+H2O?HCl+HClO | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | D. | 2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ |
4.某碳酸钠溶液中的钠离子与水分子的个数比是1:20,则该溶液的质量分数为( )
| A. | 6.4% | B. | 25.6% | C. | 12.8% | D. | 60% |
1.已知X、Y是主族元素,I为电离能,单位是kJ•mol-1.根据如表所列数据判断,错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 元素Y是IIIA族元素 | |
| C. | 若元素Y处于第3周期,它的单质可与冷水剧烈反应 | |
| D. | 元素X与氯元素形成化合物时,化学式可能是XCl |
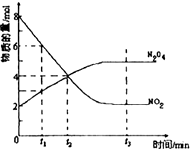 一定温度下,在容积为1L的密闭容器中放入2molN2O4和8molNO2,发生如下反应2NO2(红棕色)═N2O4(无色)△H<0反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
一定温度下,在容积为1L的密闭容器中放入2molN2O4和8molNO2,发生如下反应2NO2(红棕色)═N2O4(无色)△H<0反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答: