题目内容
9.通过用水溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )| A. | 硝酸钾、氢氧化钠 | B. | 氧化铜、二氧化锰 | C. | 氯化钾、二氧化锰 | D. | 硫酸铜、氢氧化钡 |
分析 用水溶解、过滤、蒸发等操作分离,则混合物中有一种物质不溶于水,结合物质的溶解性来解答.
解答 解:A.二者均溶于水,过滤不能分离,故A不选;
B.二者均不溶于水,过滤不能分离,故B不选;
C.KCl溶于水,二氧化锰不溶于水,用水溶解、过滤、蒸发可分离,故C选;
D.硫酸铜、氢氧化钡溶于水发生复分解反应,不能分离,故D不选;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
19.硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得. 已知:Na2S2O3在酸性溶液中不能稳定存在.
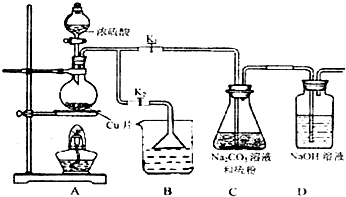
(1)某研究小组设计了制备Na2S203•5H20装置和部分操作步骤如下.
I.打开K1关闭K2,向圆底 烧瓶中加入足量浓硫酸加热.
II.C中混合液被气流搅动,反应一段时间后,硫粉逐渐减少,当C中溶液的pH 接近7时,打开K2,关闭K1即停止C中的反应,停止加热.
III.过滤C中的混合液.
IV.将滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、烘干,得到产品Na2S203.5H20.
回答下列问题:
①II中,“当C中溶液的pH接近7时即停止C中的反应”的原因S2O32-+2H+═S↓+SO2↑+H2O(用离子方程式表示).
②IV中,操作步骤是蒸发浓缩、冷却结晶.
③装置B中盛放的试剂是(填化学式)NaOH溶液.
(2)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO${\;}_{4}^{2-}$全部转化为Cr2O${\;}_{7}^{2-}$;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.0010mol.L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
部分反应离子方程式为:
①Cr2O${\;}_{7}^{2-}$+6I-+14H+═2Cr3++3I2+7H2O;
②I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$.
Ⅰ.判断达到滴定终点的现象是加入最后一滴Na2S2O3标准溶液后,蓝色消失,且半分钟内颜色不改变
Ⅱ.从表格所给数据计算:一份待测溶液消耗Na2S2O3溶液的平均体积为18.00 ml
Ⅲ.废水中Ba2+的物质的量浓度2.4×10-4mol•L-1.

(1)某研究小组设计了制备Na2S203•5H20装置和部分操作步骤如下.
I.打开K1关闭K2,向圆底 烧瓶中加入足量浓硫酸加热.
II.C中混合液被气流搅动,反应一段时间后,硫粉逐渐减少,当C中溶液的pH 接近7时,打开K2,关闭K1即停止C中的反应,停止加热.
III.过滤C中的混合液.
IV.将滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、烘干,得到产品Na2S203.5H20.
回答下列问题:
①II中,“当C中溶液的pH接近7时即停止C中的反应”的原因S2O32-+2H+═S↓+SO2↑+H2O(用离子方程式表示).
②IV中,操作步骤是蒸发浓缩、冷却结晶.
③装置B中盛放的试剂是(填化学式)NaOH溶液.
(2)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO${\;}_{4}^{2-}$全部转化为Cr2O${\;}_{7}^{2-}$;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.0010mol.L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
①Cr2O${\;}_{7}^{2-}$+6I-+14H+═2Cr3++3I2+7H2O;
②I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$.
Ⅰ.判断达到滴定终点的现象是加入最后一滴Na2S2O3标准溶液后,蓝色消失,且半分钟内颜色不改变
Ⅱ.从表格所给数据计算:一份待测溶液消耗Na2S2O3溶液的平均体积为18.00 ml
Ⅲ.废水中Ba2+的物质的量浓度2.4×10-4mol•L-1.
20. 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | △H=E2-E1 | |
| B. | 反应物断键吸收的总能量小于生成物成键释放的总能量 | |
| C. | 升高温度,不影响活化分子百分数 | |
| D. | 使用催化剂使该反应的反应热发生改变 |
17.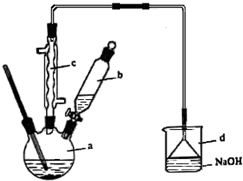 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,回答下列问题:
(1)c仪器的名称是球形冷凝管,向a中滴加几滴溴,有白雾产生,是因为生成了HBr气体,a中发生反应的化学方程式为 .该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;
.该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的目的是吸水(干燥).
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,应选择下列C操作(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)c仪器的名称是球形冷凝管,向a中滴加几滴溴,有白雾产生,是因为生成了HBr气体,a中发生反应的化学方程式为
 .该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;
.该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的目的是吸水(干燥).
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,应选择下列C操作(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
1.为配制0.01mol•L-1 的KMnO4 消毒液,下列操作导致所配溶液浓度偏高的是( )
| A. | 溶解搅拌时有液体飞溅 | |
| B. | 取KMnO4样品时不慎在表面沾了点蒸馏水 | |
| C. | 定容时俯视容量瓶刻度线 | |
| D. | 定容摇匀后见液面下降,再加水至刻度线 |
18.某溶液中可能含有Cl-、Br-、SO32-、SO42-、NH4+、Fe2+、K+中的几种离子,现取100mL该溶液加入足量的新制氯水,溶液呈无色,继续滴加稀盐酸,无气泡产生;再往其中加入BaCl2溶液,产生白色沉淀,沉淀经过滤、洗涤、干燥后质量为4.66g.滤液加足量氢氧化钠溶液、加热,生成气体在标准状况下体积为448mL.最后向剩余沉淀中加入HNO3酸化的AgNO3溶液,有白色沉淀生成.根据上述实验现象,以下推测正确的是( )
| A. | 原溶液中一定存在SO42-、NH4+、Cl- | |
| B. | 原溶液中一定不存在Br-、Fe2+、SO32- | |
| C. | 原溶液中可能存在SO32-、K+ | |
| D. | 原溶液中滴定存在K+,c(K+)≥0.2mol•L-1 |
19.下列各项与化学平衡移动原理无关的是( )
| A. | 收集Cl2用排饱和食盐水的方法 | |
| B. | 加催化剂,使SO2和O2 在一定条件下转化为SO3 | |
| C. | 可用浓氨水和NaOH(s)快速制取氨气 | |
| D. | 加压条件下有利于N2和H2反应生成NH3 |

 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):