题目内容
10.某溶液中含有较大量的Cl-、CO32-、SO42-3种阴离子,请设计实验,要求只取一次该溶液就能够分别将3种阴离子依次检验出来,按加入顺序写出所加的试剂的化学式HNO3、Ba(NO3)2、AgNO3.分析 Cl-与银离子结合生成沉淀,CO32-与酸反应生成气体,SO42-与钡离子结合生成沉淀,结合只取一次该溶液就能够分别将3种阴离子依次检验出来来解答.
解答 解:因检验氯离子可以使用银离子,检验硫酸根离子可以使用钡离子,检验碳酸根离子可以使用氢离子,而银离子和钡离子都可以与碳酸根离子结合成沉淀,所以需先检验碳酸根离子,此时可以加入稀硝酸,反应的离子方程式为CO32-+2H+=H2O+CO2↑,检验氯离子所用的银离子可以与硫酸根离子结合成微溶于水的硫酸银,所以需先检验硫酸根离子,此时可以加入硝酸钡,最后检验氯离子,可以加入硝酸银,反应生成沉淀,反应的离子方程式为Ag++Cl-=AgCl↓.
故答案为:HNO3、Ba(NO3)2、AgNO3.
点评 本题考查物质的鉴别和检验,为高频考点,把握离子检验的试剂、发生的反应及现象为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
20.下列说法正确的是( )
| A. | 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 | |
| B. | 物质发生化学变化一定伴随着能量变化,且能量形式只表现为热量变化 | |
| C. | 把石墨完全转化为金刚石时,要吸收能量,所以石墨不如金刚石稳定 | |
| D. | 原子结合成分子的过程一定释放出能量 |
1.下列属于吸热反应的是( )
| A. | 镁的燃烧反应 | B. | 盐酸与氢氧化钠的反应 | ||
| C. | 水的分解反应 | D. | 铝与盐酸的反应 |
18.下列有关说法正确的是( )
| A. | 氨水稀释后,溶液中$\frac{c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值减小 | |
| B. | 0.1 mol•L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小 | |
| C. | 298 K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H<0 | |
| D. | 对N2(g)+3H2(g)═2NH3(g),其他条件不变时充入N2,正反应速率增大,逆反应速率减小 |
5.过氧化钙晶体CaO2•8H2O较稳定,呈白色,微溶于水,能溶于酸性溶液.广泛应用于环境杀菌、消毒等领域.过氧化钙晶体含量的测定(假定杂质不发生反应)
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol•L-1 H2SO4,
发生化学反应:CaO2•8H2O+H2SO4═CaSO4+H2O2+8H2O用0.0200mol•L-1KMnO4
标准溶液滴定至终点.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O重复上述操作两次.
(1)在滴定过程中,没有选用指示剂是因为高锰酸钾未过量前,溶液是无色的,当溶液变成浅红色.
(2)滴定终点观察到的现象为当滴入最后一滴KMnO4标准溶液后溶液由无色变浅红色,且30s不褪色.
(3)根据表中的数据,计算产品中CaO2•8H2O的质量分数(写出计算过程)
(4)用KMnO4溶液做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,若用放置了两周的KMnO4标准溶液去测定产品中CaO2•8H2O的质量分数,则测得的值将偏高(填“偏高”或“偏低”)
准确称取0.3000g产品于锥形瓶中,加入30mL蒸馏水和10mL 2.000mol•L-1 H2SO4,
发生化学反应:CaO2•8H2O+H2SO4═CaSO4+H2O2+8H2O用0.0200mol•L-1KMnO4
标准溶液滴定至终点.H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O重复上述操作两次.
(1)在滴定过程中,没有选用指示剂是因为高锰酸钾未过量前,溶液是无色的,当溶液变成浅红色.
(2)滴定终点观察到的现象为当滴入最后一滴KMnO4标准溶液后溶液由无色变浅红色,且30s不褪色.
(3)根据表中的数据,计算产品中CaO2•8H2O的质量分数(写出计算过程)
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 26.04 |
| 2 | 0.3000 | 2.00 | 25.02 |
| 3 | 0.3000 | 0.20 | 23.24 |
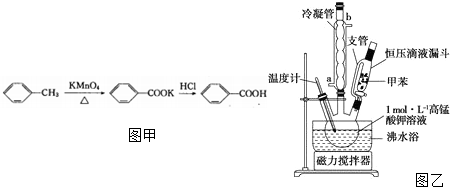
15.苯甲酸是一种重要的化工原料,某学习小组设计方案制备苯甲酸,合成苯甲酸的原理、一个数据及装置示意图如图甲:
注释:苯甲酸在100g水中的溶解度为:4℃,0.18g;18℃,0.27g;75℃,2.2g.
按下列合成步骤回答问题:
Ⅰ.苯甲酸制备:(1)按如图乙所示以三颈烧瓶为反应器,用30.0mL甲苯和25.0mL 1mol•L-1高锰酸钾溶液在80℃下反应30min,静置发现不再出现分层现象时,停止反应.装置中a是将甲苯和水冷凝回流,防止甲苯的挥发而降低产品产率.(填进水管或出水管)图中支管的作用是平衡压强,便于甲苯顺利滴入三颈烧瓶.
Ⅱ.分离提纯.
(2)在反应后的混合物中加入一定量亚硫酸氢钠溶液充分反应使紫色褪去,此时反应的离子方程式为2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2H2O.
(3)过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,除杂.产品减压过滤时用冷水洗涤的原因是苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失,把制得的苯甲酸粗产品进一步提纯,可用下列D操作(填字母)
A.溶于水后过滤 B.溶于乙醇后蒸馏C.用甲苯萃取后分液 D.升华.
Ⅲ.产品纯度测定.
(4)称取1.220g产品,配成100mL乙醇溶于,移取25.00mL溶于于锥形瓶中,滴加2-3滴酚酞(填写“甲基橙”或“酚酞”),然后用0.1000mol•L-1KOH溶液滴定,滴定终点溶液的颜色变化是溶液颜色由无色变为浅红色,且30S内不褪色.到达滴定终点时消耗KOH溶液24.00mL(苯甲酸的相对分子质量:122).产品中苯甲酸质量分数为96.00%.
| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 112.4 (100℃左右升华) | 248 | 1.2659 | 微溶 | 易溶 |
按下列合成步骤回答问题:
Ⅰ.苯甲酸制备:(1)按如图乙所示以三颈烧瓶为反应器,用30.0mL甲苯和25.0mL 1mol•L-1高锰酸钾溶液在80℃下反应30min,静置发现不再出现分层现象时,停止反应.装置中a是将甲苯和水冷凝回流,防止甲苯的挥发而降低产品产率.(填进水管或出水管)图中支管的作用是平衡压强,便于甲苯顺利滴入三颈烧瓶.
Ⅱ.分离提纯.
(2)在反应后的混合物中加入一定量亚硫酸氢钠溶液充分反应使紫色褪去,此时反应的离子方程式为2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2H2O.
(3)过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,除杂.产品减压过滤时用冷水洗涤的原因是苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失,把制得的苯甲酸粗产品进一步提纯,可用下列D操作(填字母)
A.溶于水后过滤 B.溶于乙醇后蒸馏C.用甲苯萃取后分液 D.升华.
Ⅲ.产品纯度测定.
(4)称取1.220g产品,配成100mL乙醇溶于,移取25.00mL溶于于锥形瓶中,滴加2-3滴酚酞(填写“甲基橙”或“酚酞”),然后用0.1000mol•L-1KOH溶液滴定,滴定终点溶液的颜色变化是溶液颜色由无色变为浅红色,且30S内不褪色.到达滴定终点时消耗KOH溶液24.00mL(苯甲酸的相对分子质量:122).产品中苯甲酸质量分数为96.00%.

4.中和热的测定实验中,可能用到下列仪器.其中应使用仪器的正确组合是( )
①托盘天平 ②量筒 ③烧杯 ④温度计 ⑤小试管 ⑥酒精灯.
①托盘天平 ②量筒 ③烧杯 ④温度计 ⑤小试管 ⑥酒精灯.
| A. | ①②⑤ | B. | ②③④ | C. | ②③⑥ | D. | 全部 |
1.建构数学模型来研究化学问题,既直观又简洁.下列建构的数轴模型正确的是( )
| A. | 钠在氧气中燃烧,钠的氧化产物: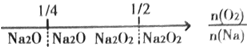 | |
| B. | 铁在Cl2中燃烧,铁的氧化产物: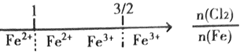 | |
| C. | A1Cl3溶液中滴加NaOH溶液后体系中铝元素的存在形式: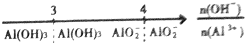 | |
| D. | FeI2溶液中通入Cl2,铁元素存在形式: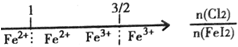 |
2.芳香族化合物G与 互为同分异构体,G的苯环上的一氯代物只有一种结构,则G可能的结构有( )
互为同分异构体,G的苯环上的一氯代物只有一种结构,则G可能的结构有( )
 互为同分异构体,G的苯环上的一氯代物只有一种结构,则G可能的结构有( )
互为同分异构体,G的苯环上的一氯代物只有一种结构,则G可能的结构有( )| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |