题目内容
下列判断错误的是( )
| A、NO2可与水反应 |
| B、Al(OH)3是既能与强酸反应又能与强碱反应,是两性氢氧化物 |
| C、金属钠投入硫酸铜溶液中可置换出金属铜 |
| D、NaHCO3俗称是小苏打,可用作食用碱 |
考点:氮的氧化物的性质及其对环境的影响,钠的化学性质,钠的重要化合物,镁、铝的重要化合物
专题:元素及其化合物
分析:A、NO2可与水反应生成硝酸和一氧化氮;
B、Al(OH)3是两性氢氧化物,既能与强酸反应又能与强碱反应;
C、金属钠投入硫酸铜溶液中先与水反应生成氢氧化钠;
D、NaHCO3俗称是小苏打,可用作食用碱.
B、Al(OH)3是两性氢氧化物,既能与强酸反应又能与强碱反应;
C、金属钠投入硫酸铜溶液中先与水反应生成氢氧化钠;
D、NaHCO3俗称是小苏打,可用作食用碱.
解答:
解:A、NO2可与水反应生成硝酸和一氧化氮,故A正确;
B、Al(OH)3是两性氢氧化物,既能与强酸反应又能与强碱反应,故B正确;
C、金属钠投入硫酸铜溶液中先与水反应生成氢氧化钠,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠溶液,不会置换出金属铜,故C错误;
D、食用碱成分为NaHCO3,俗称是小苏打,故D正确.
故选:C.
B、Al(OH)3是两性氢氧化物,既能与强酸反应又能与强碱反应,故B正确;
C、金属钠投入硫酸铜溶液中先与水反应生成氢氧化钠,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠溶液,不会置换出金属铜,故C错误;
D、食用碱成分为NaHCO3,俗称是小苏打,故D正确.
故选:C.
点评:本题考查内容较为综合,注意金属钠投入水溶液中首先和水反应生成氢氧化钠,氢氧化钠在去和溶液中的溶质反应.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中正确的是( )
| A、根据化合价Fe3O4可表示为FeO?Fe2O3,则Fe3I8也可表示为FeI2?2FeI3 |
| B、CaC2能水解:CaC2+2H2O→Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O→4Al(OH)3↓+3CH4↑ |
| C、O2与Cu反应加热生成CuO,则S与Cu反应加热生成CuS |
| D、SO2通入BaCl2溶液中不产生沉淀,则SO2通入Ba(NO3)2溶液中也不产生沉淀 |
下列叙述不正确的是( )
| A、乙醇、乙烯和植物油都能使酸性高锰酸钾褪色 |
| B、乙醇、乙烷、乙酸都可以与钠反应生成氢气 |
C、聚丙烯的结构简式为: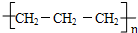 |
| D、用灼烧闻气味的方法可以区分纯棉织物和纯毛织物 |
可逆反应达到平衡的根本原因是( )
| A、反应混合物中各组分的浓度相等 |
| B、正逆反应都还在继续进行 |
| C、正逆反应的速率均为零 |
| D、化学平衡理论是研究怎样使原料尽可能多地转化为产品 |
25℃时,将a mol/L的氨水与b mol/L盐酸等体积混合,下列有关推论不正确的是( )
| A、若混合后溶液pH=7,则c(NH4+)═c(Cl-) |
| B、若b=2a,则c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、若a=2b,则(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、若混合后溶液满足c(H+)═c(OH-)+c(NH3?H2O),则可推出a=b |
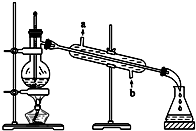 甘油的分离
甘油的分离