题目内容
按要求写化学方程式
①燃烧天然气
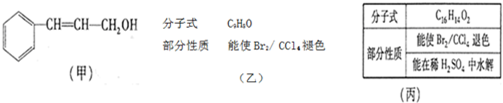
②乙烯与水反应
③苯与溴反应
④苯与浓硝酸反应
⑤乙醇的催化氧化 .
①燃烧天然气
②乙烯与水反应
③苯与溴反应
④苯与浓硝酸反应
⑤乙醇的催化氧化
考点:有机化学反应的综合应用
专题:有机反应
分析:①天然气的主要成分为甲烷,甲烷在空气中燃烧生成二氧化碳和水;
②乙烯不饱和的C=C双键中,其中1个C-C断裂结合水提供的-H、-OH,发生加成反应;
③苯和液溴在铁粉作催化剂条件下反应生成溴苯和溴化氢;
④苯与浓硝酸在催化剂存在条件下加热反应生成硝基苯;
⑤乙醇在催化剂存在条件下加热与氧气反应生成乙醛和水.
②乙烯不饱和的C=C双键中,其中1个C-C断裂结合水提供的-H、-OH,发生加成反应;
③苯和液溴在铁粉作催化剂条件下反应生成溴苯和溴化氢;
④苯与浓硝酸在催化剂存在条件下加热反应生成硝基苯;
⑤乙醇在催化剂存在条件下加热与氧气反应生成乙醛和水.
解答:
解:①天然气的主要成分是甲烷,甲烷和氧气在点燃的条件下生成二氧化碳和水,反应的化学方程式为:CH4+2O2
CO2+2H2O,
故答案为:CH4+2O2
CO2+2H2O;
②CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇,反应的化学方程式为:CH2=CH2+H2O
CH3CH2OH,
故答案为:CH2=CH2+H2O
CH3CH2OH;
③在催化剂的作用下,苯环上的氢原子溴原子所取代,生成溴苯,同时有溴化氢生成:C6H6+Br2
C6H5Br+HBr,
故答案为:C6H6+Br2
C6H5Br+HBr;
④苯与浓硝酸在浓硫酸存在条件下加热发生反应生成硝基苯,反应的化学方程式为: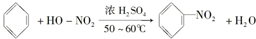 ,
,
故答案为: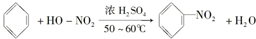 ;
;
⑤乙醇催化氧化,生成乙醛和水,反应方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O.
| ||
故答案为:CH4+2O2
| ||
②CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇,反应的化学方程式为:CH2=CH2+H2O
| 催化剂 |
故答案为:CH2=CH2+H2O
| 催化剂 |
③在催化剂的作用下,苯环上的氢原子溴原子所取代,生成溴苯,同时有溴化氢生成:C6H6+Br2
| Fe |
故答案为:C6H6+Br2
| Fe |
④苯与浓硝酸在浓硫酸存在条件下加热发生反应生成硝基苯,反应的化学方程式为:
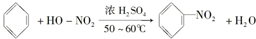 ,
,故答案为:
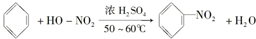 ;
;⑤乙醇催化氧化,生成乙醛和水,反应方程式为:2CH3CH2OH+O2
| Cu |
| △ |
故答案为:2CH3CH2OH+O2
| Cu |
| △ |
点评:本题考查了有机反应方程式的书写,为高频考点,题目难度中等,注意掌握常见有机物结构与性质,根据反应原理找出正确的反应物、生成物、反应条件为解答关键.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
某蓄电池放电、充电时反应为:Fe+Ni2O3+3H2O
Fe(OH)2+2Ni(OH)2,下列推断不正确的是( )
| 放电 |
| 充电 |
| A、放电时,负极上的电极反应式是:Fe+2OH--2e-=Fe(OH)2 |
| B、放电时,每转移2 mol 电子,正极上有1 mol Ni2O3被氧化 |
| C、充电时,阳极上的电极反应式是:2Ni(OH)2-2e-+2OH-=Ni2O3+3H2O |
| D、该蓄电池的电极必须是浸在某种碱性电解质溶液中 |
下列各组混合物,其总的物质的量均为a mol,组内各物质的物质的量以任意比混合,完全燃烧时消耗O2的量不变的是( )
| A、乙炔、乙醛、乙二醇 |
| B、乙烯、乙酸、葡萄糖 |
| C、乙烯、丁烯、环已烷 |
| D、乙烯、乙醇、丙烯酸 |
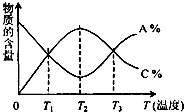 已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 (两个答案)( )
已知可逆反应aA+bBcC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 (两个答案)( )| A、该反应在T1、T3温度时达到过化学平衡 |
| B、该反应在T2温度时达到过化学平衡 |
| C、该反应的逆反应是吸热反应 |
| D、升高温度,平衡会向正反应方向移动 |
下列判断错误的是( )
| A、NO2可与水反应 |
| B、Al(OH)3是既能与强酸反应又能与强碱反应,是两性氢氧化物 |
| C、金属钠投入硫酸铜溶液中可置换出金属铜 |
| D、NaHCO3俗称是小苏打,可用作食用碱 |