题目内容
7.下列说法正确的是( )| A. | 将AlCl3溶液加热蒸干得到纯净的氯化铝晶体 | |
| B. | 在一定条件下,反应N2+3H2?2NH3,在2L密闭容器中进行,5min内氨的物质的量增加了lmol,则该反应的速率可表示为v(NH3)=0.2mol•L-1•min-1 | |
| C. | 强酸溶液一定比弱酸溶液导电性强 | |
| D. | 钢铁在表层海水中的腐蚀速率大于在潮湿空气中的腐蚀速率 |
分析 A.加热条件下,AlCl3易水解生成氢氧化铝;
B.根据c=$\frac{△c}{△t}$计算;
C.导电性与溶液中离子浓度大小有关;
D.表层海水离子浓度较大,导电性强.
解答 解:A.加热条件下,AlCl3易水解,可生成氢氧化铝,如灼烧,则生成氧化铝,故A错误;
B.c=$\frac{△c}{△t}$=$\frac{\frac{1mol}{2L}}{5min}$=0.1mol•L-1•min-1,故B错误;
C.导电性与溶液中离子浓度大小有关,强电解质的浓度如较小,则导电能力也许比弱电解质弱,故C错误;
D.表层海水离子浓度较大,导电性强,形成原电池反应,故D正确.
故选D.
点评 本题考查较为综合,为高考常见题型,涉及盐类的水解、化学反应速率,电解质的电离以及金属的腐蚀等问题,综合考查化学反应原理问题,注意相关知识的学习,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.往浅绿色的Fe(NO3)2溶液中逐滴加入盐酸时,溶液颜色( )
| A. | 绿色逐渐变浅 | B. | 绿色逐渐加深 | C. | 没有改变 | D. | 变黄色 |
18.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 用玻璃杯蘸取某溶液进行焰火反应实验 | 火焰呈黄色 | 溶液中含有Na+ |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D | 用Fe3+浓度相同的FeCl3溶液和Fe2(SO4)3溶液,分别用于清洗做完眼镜反应的试管 | 用FeCl3溶液清洗比Fe2(SO4)3溶液清洗得干净 | Fe3+氧化银单质的过程可能是一个可逆过程: Fe3++Ag?Fe2++Ag+ |
| A. | A | B. | B | C. | C | D. | D |
15.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 46g组成为C2H6O的有机物,所含有的C-H键数目为6NA | |
| B. | 0℃18mL冰含有质子数为10NA | |
| C. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| D. | 0.3molZn与一定量浓硫酸恰好完全反应,生成气体的分子数为0.3NA |
2.有四种微粒的结构示意图如图,下列说法错误的是( )
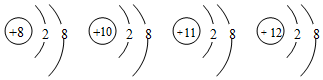
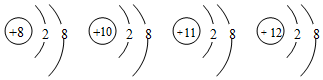
| A. | 它们属于不同种元素 | |
| B. | 它们的核外电子排布相同 | |
| C. | 它们都是离子 | |
| D. | 它们都具有稀有气体原子的稳定结构 |
12.下列属于碱的是( )
| A. | HClO | B. | CO2 | C. | Na2CO3 | D. | Ca(OH)2 |
19.下列不属于物质分离、提纯实验操作用到的实验装置是( )
| A. | 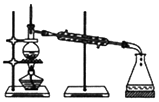 | B. | 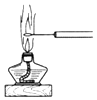 | ||
| C. | 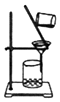 | D. | 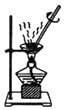 |
16.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4═Na2SO4+SO2↑+S↓+H2O,可以通过出现浑浊的快慢来判断反应的快慢程度,下列各组实验中最先出现浑浊的是( )
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | ||
| V/mL | c/(mol•L-1) | V/mL | c/(mol•L-1) | ||
| A | 25 | 5 | 0.1 | 20 | 0.1 |
| B | 25 | 5 | 0.2 | 10 | 0.2 |
| C | 35 | 5 | 0.1 | 20 | 0.1 |
| D | 35 | 5 | 0.2 | 10 | 0.2 |
| A. | A | B. | B | C. | C | D. | D |
17.近年来,全国安全事故频发,折射出人们对化学品与安全知识的极度缺乏,下列有关化学品与安全的说法或操作错误的是( )
| A. | A.运石油的油罐车上应贴  标志,并由专人押运 标志,并由专人押运 | |
| B. | 不慎将酒精洒到桌面上引起着火,可用水扑灭 | |
| C. | 氢氧化钠浓溶液溅入眼中,应立即用大量水冲洗,再用硼酸稀溶液冲洗 | |
| D. | 右图装置可分离CH3COOC2H5和碳酸钠饱和溶液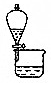 |