题目内容
19.下列不属于物质分离、提纯实验操作用到的实验装置是( )| A. | 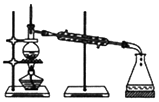 | B. | 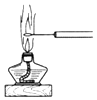 | ||
| C. | 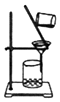 | D. | 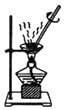 |
分析 A.图中为蒸馏装置;
B.图中为焰色反应;
C.图中为过滤装置;
D.图中为蒸发装置.
解答 解:A.蒸馏可分离互溶液体、但沸点不同的混合物,故A不选;
B.焰色反应可检验某些金属元素,故B选;
C.过滤可分离不溶性固体与液体,故C不选;
D.蒸发可分离可溶性固体与液体,故D不选;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
5.下列金属中,表面自然能形成致密的氧化层能保护内层金属不被空气氧化的是( )
| A. | 金 | B. | 钠 | C. | 铁 | D. | 铝 |
10.已知NO2和溴蒸气都是红棕色气体,且都有强氧化性,则下列试剂或方法不能将NO2和溴蒸气区别开的是( )
| A. | 向两种气体中加入适量水,振荡 | B. | 将两种气体分别通入AgNO3溶液中 | ||
| C. | 用湿润的淀粉KI试纸检验 | D. | 将两种气体分别通入FeCl2溶液中 |
7.下列说法正确的是( )
| A. | 将AlCl3溶液加热蒸干得到纯净的氯化铝晶体 | |
| B. | 在一定条件下,反应N2+3H2?2NH3,在2L密闭容器中进行,5min内氨的物质的量增加了lmol,则该反应的速率可表示为v(NH3)=0.2mol•L-1•min-1 | |
| C. | 强酸溶液一定比弱酸溶液导电性强 | |
| D. | 钢铁在表层海水中的腐蚀速率大于在潮湿空气中的腐蚀速率 |
14.下列说法不正确的是( )
| A. | 用烧杯可以精确配制0.1mol/L的NaOH溶液 | |
| B. | 用淀粉溶液检验某溶液中是否存在碘单质 | |
| C. | 可利用丁达尔效应区分胶体与溶液 | |
| D. | 用苯可以萃取溴水中的溴单质 |
4.下列物质中的主要成分不是硅酸盐的是( )
| A. | 玻璃 | B. | 陶瓷 | C. | 石英 | D. | 水泥 |
11.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应发生过程中要不断从外界获得能量,放热反应不需要吸收外界能量 | |
| D. | 是放热反应还是吸热反应主要由反应物、生成物所具有的总能量的相对大小决定 |
8.一定温度下.在3个体积均为1.0L的恒容器密闭容器中反应2H2(g)+CO(g)?CH3O g)达到平衡,已知Ⅰ中的反应经过40min后达到平衡,则下列说法正确的是( )
| 容器 | 温度/k | 物质的起始浓度/mol•L-1 | CH3OH的平衡浓度/mol•L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | |||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | Ⅰ中反应在0-40min内的平均速率为υ(H2)=0.0020mol•L-1•min-1 | |
| B. | 达到平衡时,容器Ⅰ中的反应物转化率比容器Ⅱ中的大 | |
| C. | 三个容器中反应的平衡常数关系为Ⅱ=Ⅰ>Ⅲ | |
| D. | 达若起始时向容器Ⅰ中充入0.020molH2、0.010molCO和0.010molCH3OH |
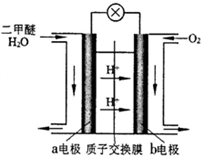 二甲醚(CH3OCH3)是一种清洁、高效、具有优良的环保性能的可燃物,被称为21世纪的新型能源.工业制备二甲醚的生产流程如下:
二甲醚(CH3OCH3)是一种清洁、高效、具有优良的环保性能的可燃物,被称为21世纪的新型能源.工业制备二甲醚的生产流程如下: