题目内容
10.写出下列化学反应的离子方程式①氢氧化钡溶液和硫酸溶液反应Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
②碳酸钙和足量稀盐酸反应CaCO3+2H+=Ca2++CO2↑+H2O
③碳酸氢钠和稀盐酸反应HCO3-+H+=H2O+CO2↑.
分析 ①氢氧化钡溶液和硫酸溶液反应生成硫酸钡和水;
②碳酸钙和足量稀盐酸反应生成氯化钙和二氧化碳、水;
③碳酸氢钠和稀盐酸反应生成氯化钙和水、二氧化碳.
解答 解:①氢氧化钡溶液和硫酸溶液反应生成硫酸钡和水,离子方程式:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;
②碳酸钙和足量稀盐酸反应生成氯化钙和二氧化碳、水,离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
③碳酸氢钠和稀盐酸反应生成氯化钙和水、二氧化碳,离子方程式为:HCO3-+H+=H2O+CO2↑;
故答案为:HCO3-+H+=H2O+CO2↑.
点评 本题考查了离子方程式的书写,题目难度中等,注意掌握离子方程式的概念、表示意义及书写原则,明确需要保留化学式的物质,如难溶物、弱电解质、氧化物,还要区别离子方程式满足守恒关系,如:质量守恒定律、电荷守恒、电子守恒.

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
7.在一定条件下,将A2和B2两种气体通入1L密闭容器中,发生反应:xA2(g)+yB2(g)?2C(g),2S内的反应速率:V (A2)=0.5mol•L-1•s-1,V (B2)=1.5mol•L-1•s-1,V (C)=1mol•L-1•s-1 则x和y的值分别为( )
| A. | 2和3 | B. | 3和2 | C. | 3和1 | D. | 1和3 |
1.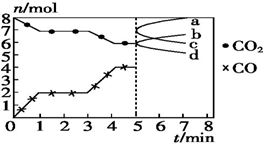 炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)═2CO(g)△H=Q kJ•mol-1.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )
炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)═2CO(g)△H=Q kJ•mol-1.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )
 炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)═2CO(g)△H=Q kJ•mol-1.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )
炼铁的还原剂CO是由焦炭和CO2反应而得.现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)═2CO(g)△H=Q kJ•mol-1.如图为CO2、CO的物质的量n随时间t的变化关系图.下列说法正确的是( )| A. | 0~1 min,v(CO)=1 mol•L-1•min-1;1~3 min,v(CO)=v(CO2) | |
| B. | 当容器内的压强不变时,反应一定达到平衡状态,$\frac{P(平衡)}{P(起始)}$<1 | |
| C. | 3 min时,温度由T1升高到T2,则Q>0,再达平衡时,$\frac{K({T}_{2})}{K({T}_{1})}$>1 | |
| D. | 5 min时再充入一定量的CO,a、b曲线分别表示n(CO)、n(CO2)的变化 |
18.恒容密闭容器中,某化学反应2A?B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如表:
根据上述数据,完成下列填空:
(1)在实验1,反应在前20min内用B的浓度变化来表示的平均速率为0.009mol/(L•min).
(2)在实验2,A的初始浓度c2=1.0mol/L,反应在 20分钟内就达到平衡,可推测实验2中还隐含的条件是加入催化剂.
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1(用同种物质的浓度变化表示),则达到平衡时υ3>υ1(填>、=、<=)且c3=1.2 mol/L.
(4)比较实验4和实验1,可推测该反应是吸热反应(选填“吸热”、“放热”).
(5)800℃时,反应2A?B+D的平衡常数=0.25,实验2中达到平衡时A的转化率=50%.
| 实验序号 | 浓度(mol/L) | 时间(min) | |||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | |||
| 1 | 温 度 | 800℃ | 1.0 | 0.80 | O.64 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 | |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 | |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 | |
(1)在实验1,反应在前20min内用B的浓度变化来表示的平均速率为0.009mol/(L•min).
(2)在实验2,A的初始浓度c2=1.0mol/L,反应在 20分钟内就达到平衡,可推测实验2中还隐含的条件是加入催化剂.
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1(用同种物质的浓度变化表示),则达到平衡时υ3>υ1(填>、=、<=)且c3=1.2 mol/L.
(4)比较实验4和实验1,可推测该反应是吸热反应(选填“吸热”、“放热”).
(5)800℃时,反应2A?B+D的平衡常数=0.25,实验2中达到平衡时A的转化率=50%.
5.下列说法或对应关系中,正确的是( )
| A. | Fe比Cu的金属性强,因此可用FeCl3腐蚀Cu刻制应刷电路板 | |
| B. | 纯碱、小苏打、盐酸分别属于碱、盐、混合物 | |
| C. | 胶体化学是制造纳米材料的有效方法之一 | |
| D. | 用萃取方法分离碘的苯溶液 |
20.现有下列10种物质:
①液态氧 ②空气 ③Mg ④二氧化碳⑤H2SO4⑥Ca(OH)2⑦CuSO4•5H2O⑧牛奶 ⑨C2H5OH ⑩NaHCO3下列分类正确的是( )
①液态氧 ②空气 ③Mg ④二氧化碳⑤H2SO4⑥Ca(OH)2⑦CuSO4•5H2O⑧牛奶 ⑨C2H5OH ⑩NaHCO3下列分类正确的是( )
| A. | 属于混合物的是②⑦⑧ | B. | 属于盐的是⑥⑩ | ||
| C. | 属于电解质的是⑤⑥⑦⑩ | D. | 属于分散系的是②⑦⑧⑨ |
 Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:
Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下: