题目内容
2.为研究不同条件对反应2NO(g)+Cl2(g)?2ClNO(g)△H<0的影响,在恒温下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应达到平衡,测得NO的转化率为α1;其他条件保持不变,反应在恒压条件下进行,达到平衡时NO的转化率为α2,则α1小于α2(填“大于”“小于”或“等于”).分析 该反应的正反应是一个反应前后气体体积减小放热的反应,恒温恒容条件下,随着反应的进行,容器内压强逐渐降低但其容器容积不变;
恒温恒压条件下,随着反应的进行,容器容积逐渐减小,但其压强不变,
所以,在反应过程中,恒温恒压条件下压强始终不恒温恒容条件下的压强,增大压强平衡向气体体积减小的方向移动.
解答 解:该反应的正反应是一个反应前后气体体积减小放热的反应,恒温恒容条件下,随着反应的进行,容器内压强逐渐降低但其容器容积不变;
恒温恒压条件下,随着反应的进行,容器容积逐渐减小,但其压强不变,
所以,在反应过程中,恒温恒压条件下压强始终不恒温恒容条件下的压强,增大压强平衡向气体体积减小的方向移动,即向正反应方向移动,所以转化率α1小于α2,
故答案为:小于.
点评 本题考查化学平衡计算,侧重考查学生分析判断能力,明确反应前后改变的物理量对化学平衡影响是解本题关键,题目难度不大.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
12.下图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,下列叙述错误的是( )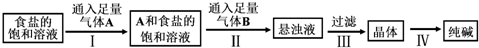
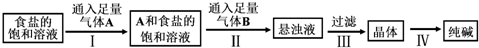
| A. | 气体A是NH3,气体B是CO2 | |
| B. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| C. | 第III步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 | |
| D. | 第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
13.在一定体积的密闭容器中,进行如下化学反应:C(s)+H2O(g)?CO(g)+H2(g),其化学平衡常数K与温度t的关系如下表:
请回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$.
(2)该反应的逆反应为吸热反应(选填“吸热”或“放热”).
(3)不能判断该反应是否达到化学平衡状态的依据是D.
A.容器内压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(H2)=c(CO)
(4)某温度下,平衡浓度符合c(CO)•c(H2)=c(H2O),试判断此时的温度为830℃.
(5)为了提高H2O(g)的转化率,可以采取的措施有:①减小压强②降低温度.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)c({H}_{2})}{c({H}_{2}O)}$.
(2)该反应的逆反应为吸热反应(选填“吸热”或“放热”).
(3)不能判断该反应是否达到化学平衡状态的依据是D.
A.容器内压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(H2)=c(CO)
(4)某温度下,平衡浓度符合c(CO)•c(H2)=c(H2O),试判断此时的温度为830℃.
(5)为了提高H2O(g)的转化率,可以采取的措施有:①减小压强②降低温度.
7.下列状态的物质,既能导电又属于电解质的是( )
| A. | 液态氯化氢 | B. | NaCl晶体 | C. | 熔融的KNO3 | D. | CuSO4溶液 |
14.向KOH溶液中通入8.96L(标准状况)氯气恰好完全反应生成三种含氯盐:0.6molKCl、0.1molKClO和X.则X是( )
| A. | 0.1molKClO4 | B. | 0.1molKClO3 | C. | 0.1molKClO2 | D. | 0.2molKClO |
11.镍镉电池在通讯、交通及日常生活中有着广泛的应用,其工作原理可以表示为:Cd+2NiO(OH)+2H2O?2Ni(OH)2+Cd(OH)2以下说法中正确的是( )
| A. | 以上反应是可逆反应 | |
| B. | 放电时,镉为正极 | |
| C. | 充电时电池上标有“+”号的电极连接电源正极 | |
| D. | 以镍镉电池为电源,电解Na2CO3溶液,当收集到气体的总体积为33.6L电池中转移了2mol电子 |
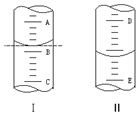 ①如图Ⅰ表示10mL量筒中液面的位置.A与B,B与C刻度间相差1mL,如果刻度A为6,量筒中液体的体积是5.2 mL.
①如图Ⅰ表示10mL量筒中液面的位置.A与B,B与C刻度间相差1mL,如果刻度A为6,量筒中液体的体积是5.2 mL.