题目内容
15. Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:
Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:步骤1.在三口烧瓶中加入白磷和石灰乳,先通入N2,然后在约98°C下充分搅拌1h,同时收集产生的PH3.
步骤2.将反应液静置、过滤.
步骤3.向滤液中通入适量CO2,再过滤.
步骤4.用次磷酸溶液调节步骤3滤液的pH,浓缩、冷却结晶、干燥得次磷酸钙.
(1)步骤1先通入N2的目的是排除装置内的空气,防止次磷酸钙及白磷被氧化;搅拌的目的是使反应物充分接触反应,加快反应速率.
(2)步骤1石灰乳与 P4(白磷)发生反应的化学方程式为2P4+3Ca(OH)2+6H2O $\frac{\underline{\;98°C\;}}{\;}$ 3Ca(H2PO2)2+2PH3↑;步骤2过滤所得滤渣成分为P4和Ca(OH)2.
(3)步骤3的目的是除去其中的Ca(OH)2.
(4)请补充完整由产品进一步制备NaH2PO2•H2O的实验方案:取产品次磷酸钙加入烧杯中,加适量的水溶解,边搅拌边向溶液中加入Na2CO3溶液,静置,向上层清液中滴入Na2CO3溶液,若无沉淀,过滤,将滤液减压蒸发浓缩,结晶,干燥得到NaH2PO2•H2O.
(已知:在常压下,加热蒸发次磷酸钠溶液会发生爆炸,100℃时NaH2PO2•H2O的溶解度为667g/100g水)
分析 (1)根据次磷酸钙及白磷易被氧化分析通入N2的目的;搅拌的目的是使反应物充分接触反应,加快反应速率;
(2)根据实验原理步骤1石灰乳与 P4(白磷)发生反应生成Ca(H2PO2)2和PH3;根据滤渣不溶于水分析步骤2过滤所得滤渣成分;
(3)步骤3向滤液中通入适量CO2,消耗溶解于水的少量Ca(OH)2;
(4)根据次磷酸钙与Na2CO3溶液反应生成碳酸钙沉淀和NaH2PO2溶液,再结合在常压下,加热蒸发次磷酸钠溶液会发生爆炸,100℃时NaH2PO2•H2O的溶解度为667g/100g水分析要得到NaH2PO2•H2O晶体的方法为减压蒸发浓缩,结晶.
解答 解:(1)因为次磷酸钙及白磷易被氧化,所以步骤1先通入N2的目的是排除装置内的空气,防止次磷酸钙及白磷被氧化;搅拌的目的是使反应物充分接触反应,加快反应速率,
故答案为:排除装置内的空气,防止次磷酸钙及白磷被氧化;使反应物充分接触反应,加快反应速率;
(2)根据实验原理步骤1石灰乳与 P4(白磷)发生反应生成Ca(H2PO2)2和PH3,反应的化学方程式为:2P4+3Ca(OH)2+6H2O $\frac{\underline{\;98°C\;}}{\;}$ 3Ca(H2PO2)2+2PH3↑;反应后过量的P4和Ca(OH)2难溶于水,所以步骤2过滤所得滤渣成分为P4和Ca(OH)2,
故答案为:2P4+3Ca(OH)2+6H2O $\frac{\underline{\;98°C\;}}{\;}$ 3Ca(H2PO2)2+2PH3↑;P4和Ca(OH)2;
(3)因为滤液中溶有少量的Ca(OH)2,所以通入适量CO2,目的是除去其中的Ca(OH)2,故答案为:除去其中的Ca(OH)2;
(4)因为次磷酸钙与Na2CO3溶液反应生成碳酸钙沉淀和NaH2PO2溶液,所以应先加入Na2CO3溶液使次磷酸钙完全转化为碳酸钙沉淀和NaH2PO2溶液,再根据在常压下,加热蒸发次磷酸钠溶液会发生爆炸,所以采用减压蒸发浓缩,结晶得到NaH2PO2•H2O晶体,
故答案为:边搅拌边向溶液中加入Na2CO3溶液,静置,向上层清液中滴入Na2CO3溶液,若无沉淀,过滤,将滤液减压蒸发浓缩,结晶.
点评 本题考查了以白磷和石灰乳为原料制备Ca(H2PO2)2的实验原理,关键在于对每一步骤的理解和知识的迁移运用,本题难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 软水是不含Ca2+、Mg2+的水 | |
| B. | 石灰-纯碱法中石灰是指CaCO3 | |
| C. | 石灰-纯碱法软化硬水过程中,Mg2+引起的硬度转化成了Ca2+的硬度 | |
| D. | 离子交换剂不能再生 |
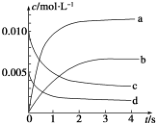 在 2L 容积不变的密闭容器内,800℃时反应 2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:
在 2L 容积不变的密闭容器内,800℃时反应 2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2浓度变化的曲线是b(填字母).
(3)能说明该反应已达到平衡状态的是BC(填序号).
A.v(NO2)=2v(O2)
B.容器内的压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内气体密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是C(填序号).
A.及时分离出NO2
B.适当升高温度
C.增大O2的浓度
D.选择高效催化剂.
| A. | 用C表示该反应的速率为0.03mol/(L•s) | |
| B. | 达到平衡,测得放出热量为x kJ,则x=Q | |
| C. | 若向容器中再充入1 mol C,重新达到平衡,A的体积分数保持不变 | |
| D. | 若升高温度,则V (逆)增大,V(正)减小,平衡逆向移动 |
| A. | 液态氯化氢 | B. | NaCl晶体 | C. | 熔融的KNO3 | D. | CuSO4溶液 |
| A. | 干电池 | B. | 铅蓄电池 | C. | 燃料电池 | D. | 锂离子电池 |
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l);△H=-57.3kJ/mol(中和热) | |
| C. | S(s)+O2(g)═SO2(g);△H=-269.8kJ/mol(反应热) | |
| D. | 2NO2═O2+2NO;△H=+116.2kJ/mol(反应热) |