题目内容
6.下列有机化合物中同分异构体数目最多的是(不考虑立体异构)( )| A. | 丁烯 | B. | 戊烷 | C. | 丙醇 | D. | 二氯甲烷 |
分析 A.丁烯存在官能团位置异构和碳链异构,还有种类异构;
B.戊烷只存在碳链异构;
C.丙醇的分子式为C3H80,碱去官能团-OH,剩下的烃基为C3H7-,所以属于醇的同分异构体有正丙醇和异丙醇,另外还有种类异构,是甲乙醚;
D.根据甲烷是正四面体结构可知二氯甲烷不存在同分异构体.
解答 解:A.丁烯存在官能团位置异构和碳链异构,分别是CH2=CHCH2CH3,CH3CH=CHCH3,CH2=C(CH3)2,种类异构还有2种,分别是环丁烷、1-甲基环丙烷,所以丁烯的同分异构体共有5种;
B.戊烷只存在碳链异构,分别是:正戊烷:CH3CH2CH2CH2CH3,2-甲基丁烷:CH3CH2CH(CH3)2,2,2-二甲基丙烷:CH3C(CH3)3,戊烷的同分异构体共有3种;
C.丙醇的分子式为C3H80,碱去官能团-OH,剩下的烃基为C3H7-,丙基有正丙基和异丙基,所以属于醇类的同分异构体有正丙醇和异丙醇,另外还有种类异构,有1种是甲乙醚,
结构简式分别是CH3CH2CH2CH2OH,CH3CHOHCH3,CH3OCH2CH3,丙醇的同分异构体共有3种;
D.根据甲烷是正四面体结构可知二氯甲烷不存在同分异构体;
故选A.
点评 本题考查了同分异构体数目的求算,题目难度中等,明确同分异构体的书写原则为解答关键,试题侧重考查学生灵活应用基础知识的能力.

练习册系列答案
相关题目
16.下列有关性质的比较,不正确的是( )
| A. | 酸性强弱:HI>HBr>HCl | B. | 非金属性:O>S>Se | ||
| C. | 还原性强弱:F->Cl->I- | D. | 碱性强弱:KOH>NaOH>LiOH |
17.下面表格中的实验操作、实验现象和结论均正确且相符的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸只表现脱水性 |
| B | 将盐酸滴入Na2CO3溶液中 | 有气泡产生 | 氯的非金属性比碳强 |
| C | 向某溶液中加入浓NaOH溶液并加热, 在试管口用湿润的红色石蕊试纸检验 | 试纸变蓝 | 原溶液中含有NH4+ |
| D | SO2通入品红溶液中 | 溶液褪色 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
1.下列说法中错误的是( )
| A. | 不是所有的烷烃中都既有极性键,又有非极性键 | |
| B. | 所有的烯烃中都是既有极性键,又有非极性键 | |
| C. | 在CCl4中碳元素呈现+4价 | |
| D. | 有机化学反应只能发生在极性键上 |
11.1mol丙醇与3mol乙酸在一定条件下反应生成乙酸乙酯和水,下列关于该反应的说法正确的是( )
| A. | 丙醇与乙酸的反应条件通常是浓硫酸、加热 | |
| B. | 充分反应可以生成1mol乙酸乙酯 | |
| C. | 生成的乙酸丙酯和水的物质的量之比是1:2 | |
| D. | 反应结束时,剩余2mol乙酸 |
18.《本草纲目》中的“石碱”条目下写道:“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面.”这里的“石碱”是指( )
| A. | KOH | B. | KAl(SO4)2 | C. | KHCO3 | D. | K2CO3 |
4.用中和滴定法测定某烧碱样品的纯度.有以下步骤:
(1)配制待测液:用已称好的5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液.除烧杯和玻璃棒外,还需要用到的主要仪器有1000mL容量瓶,胶头滴管;
(2)滴定过程:
①盛装0.10mol/L的盐酸标准液应该使用酸滴定管;
②滴定时双眼应注意观察注意观察锥形瓶内溶液颜色的变化;
(3)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①用蒸馏水冲洗锥形瓶,测定结果无影响;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外,测定结果偏高;
③读数时,滴定前仰视,滴定后俯视,测定结果偏低;
④装标准液之前,没有用标准液润洗滴定管,测定结果偏高;
(4)有关数据记录如下:
计算纯度:烧碱样品的纯度是80.8%(取两次实验所耗盐酸的平均值进行计算,不写计算过程)
(1)配制待测液:用已称好的5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液.除烧杯和玻璃棒外,还需要用到的主要仪器有1000mL容量瓶,胶头滴管;
(2)滴定过程:
①盛装0.10mol/L的盐酸标准液应该使用酸滴定管;
②滴定时双眼应注意观察注意观察锥形瓶内溶液颜色的变化;
(3)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①用蒸馏水冲洗锥形瓶,测定结果无影响;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外,测定结果偏高;
③读数时,滴定前仰视,滴定后俯视,测定结果偏低;
④装标准液之前,没有用标准液润洗滴定管,测定结果偏高;
(4)有关数据记录如下:
| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
5.六氟化硫分子呈正八面体(如图所示),在高电压下仍有良好的绝缘性,性质稳定,在电器工业方面有着广泛的用途,但逸散到空气中会引起强温室效应,下列有关六氟化硫的推测正确的是( )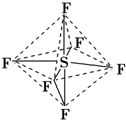

| A. | 六氟化硫中各原子均为8电子稳定结构 | |
| B. | 六氟化硫易燃烧生成二氧化硫 | |
| C. | 六氟化硫分子中含极性键、非极性键 | |
| D. | S-F键是σ键,且键长、键能都相等 |