题目内容
13.某卤代烃的结构简式如图所示: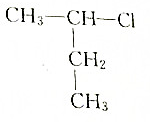
(1)写出该卤代烃的分子式:C4H9Cl.
(2)写出该卤代烃的所有同分异构体的结构式:CH2ClCH2CH2CH3、CH3CHCH2ClCH3、(CH3)3CCl;.
分析 (1)根据结构简式可知分子中含有4个C,9个H,1个Cl;
(2)C4H9Cl可以看作是丁烷中的1个H原子被Cl取代产物,先写出丁烷的同分异构体,根据等效氢判断丁烷的一氯代物种数,据此解答.
解答 解:(1)根据结构简式可知分子中含有4个C,9个H,1个Cl,分子式为C4H9Cl;
故答案为:C4H9Cl;
(2)C4H10的同分异构体有:CH3CH2CH2CH3、(CH3)3CH,
CH3CH2CH2CH3分子中有2种化学环境不同的H原子,其一氯代物有2种:CH2ClCH2CH2CH3、CH3CHClCH2CH3、
(CH3)3CH分子中有2种化学环境不同的H原子,其一氯代物有2种:CH3CHCH2ClCH3、(CH3)3CCl,
故该卤代烃的所有同分异构体的结构简式为:CH2ClCH2CH2CH3、CH3CHCH2ClCH3、(CH3)3CCl,
故答案为:CH2ClCH2CH2CH3、CH3CHCH2ClCH3、(CH3)3CCl;
点评 本题考查有机物的同分异构体的书写,难度不大,注意掌握书写方法.

 高效智能课时作业系列答案
高效智能课时作业系列答案| A. | 0.20 mol/L | B. | 0.15 mol/L | C. | 0.10 mol/L | D. | 0.05 mol/L |
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
| A. | 4种 | B. | 5种 | C. | 8种 | D. | 10种 |
a、铵盐中氮元素的化合价为-3价
b、铵盐都能水,铵盐中只含有非金属元素而不可能含有金属元素
c、铵盐都不稳定,受热分解都产生氨气
d、铵盐都是离子化合物,都能与强碱反应
e、用浓氯化铵溶液处理过的舞台幕布不易着火的原因是氯化铵分解吸收热量,降低了温度;分解产生的气体隔开了空气.
| A. | bcde | B. | abde | C. | abc | D. | ace |
| A.装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 | B.装置可除去CO2中含有的少量HCl | C.装置可制备氨气 | D.装置可制取、收集并吸收多余的HCl |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
2 mL | 0.2 mol·L?1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
0.2 mol·L?1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
0.1 mol·L?1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42?,含有Cu+、Cu2+和SO32?。
已知:Cu+ Cu +Cu2+,Cu2+
Cu +Cu2+,Cu2+ CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu2+和SO32?。

a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu+和SO32?的理由是_______________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无SO42?,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和____________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:i. Al(OH)3所吸附;ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
将对比实验方案补充完整。
步骤一:

步骤二:

则V1___________V2(填>,<或=)。
(4)根据实验,亚硫酸盐的性质有___________。盐溶液间反应的多样性与__________有关。
 2014年诺贝尔物理学奖得主的贡献是发明了一种高效而环保的光源--蓝色发光二极管(LED).某同学对此非常感兴趣,请你帮助某同学完成资料收集的工作.
2014年诺贝尔物理学奖得主的贡献是发明了一种高效而环保的光源--蓝色发光二极管(LED).某同学对此非常感兴趣,请你帮助某同学完成资料收集的工作.