题目内容
8.C5H9Cl的同分异构体可能有( )| A. | 4种 | B. | 5种 | C. | 8种 | D. | 10种 |
分析 C5H9Cl的可以看成C5H10的一氯取代产物,C5H10可能是烯烃也可能是环烷烃,若为烯烃,①先写烷烃同分异构体(烷烃碳骨架)②主链从长到短、支链由整到散、位置由心到边③“C=C”位置移动;若为环烷烃,依次减少碳环中碳原子数,当为三元环时,考虑取代基异构(2个甲基或一个乙基),根据氢原子的种类即可解答.
解答 解:C5H10可能是烯烃也可能是环烷烃,
戊烷的同分异构体有:CH3-CH2-CH2-CH2-CH3、 、
、 .
.
若为CH3-CH2-CH2-CH2-CH3,相应烯烃有CH2═CH-CH2-CH2-CH3、CH3-CH═CH-CH2-CH3,一氯代物分别有5种、5种;
若为 ,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3,一氯代物分别有4种、3种;
,相应烯烃有:CH2═C(CH3)CH2CH3;CH3C(CH3)═CHCH3,一氯代物分别有4种、3种;
若为 ,没有相应烯烃.
,没有相应烯烃.
若为环烷烃,五元环是环戊烷 ,一氯代物有1种;
,一氯代物有1种;
四元环是甲基环丁烷 ,一氯代物有4种;
,一氯代物有4种;
三元环时,存在1,2-二甲基环丙烷 ,乙基环丙烷
,乙基环丙烷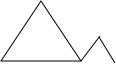 ,一氯代物分别有2种、4种;
,一氯代物分别有2种、4种;
故选AB.
点评 本题主要考查同分异构体的书写,抓住氢原子的种类=一氯代物的数目即可解答,实际上还存在顺反异构,当然需要信息的支持.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
18.下列有关说法错误的是( )
| A. |  和 和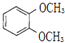 不属于同分异构体的 不属于同分异构体的 | |
| B. | 质量相同的C3H6 和C2H6完全燃烧时消耗氧气的质量较少的是C3H6 | |
| C. | 连接四个不同基团的碳原子为“手性碳原子”,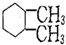 含有两个手性碳原子 含有两个手性碳原子 | |
| D. | 标准状况下22.4 L溴乙烷所含化学键总数为7NA |
19.将金属A和金属B分别放入稀H2SO4中均有氢气生成.若将金属A和金属B相连后投入稀H2SO4中发现A被腐蚀,B未被腐蚀.下列叙述正确的是( )
| A. | 金属活动性A>B | |
| B. | 还原性B>A | |
| C. | 在后者装置中金属A发生还原反应,金属B发生氧化反应 | |
| D. | 金属B的表面上明显有气泡产生,金属A表面无明显现象 |
16.0.1mol•L-1的H2S溶液中存在着电离平衡H2S?H++HS-;HS-?S2-+H+.下列叙述中错误的是( )
| A. | 从阴离子HS-电离出H+比从H2S电离出H+更难 | |
| B. | H2S电离出的H+会抑制HS-的电离 | |
| C. | 溶液中c(H+)与c(HS-)接近于相等且c(H+)略大于c(HS-) | |
| D. | 溶液中c(H+)=2c(S2-) |
13.某卤代烃的结构简式如图所示:
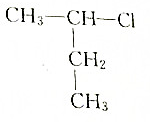
(1)写出该卤代烃的分子式:C4H9Cl.
(2)写出该卤代烃的所有同分异构体的结构式:CH2ClCH2CH2CH3、CH3CHCH2ClCH3、(CH3)3CCl;.

(1)写出该卤代烃的分子式:C4H9Cl.
(2)写出该卤代烃的所有同分异构体的结构式:CH2ClCH2CH2CH3、CH3CHCH2ClCH3、(CH3)3CCl;.
20.利用如图所示装置进行实验,通入Cl2前装置Ⅰ中溶液呈红色.下列说法不合理的是( )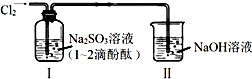

| A. | 通入Cl2后,装置Ⅰ中发生了氧化还原反应 | |
| B. | Cl2与Na2SO3溶液反应的离子方程式是:SO32-+Cl2+H2O=SO42-+2Cl-+2H+ | |
| C. | 导气管末端不应该伸入到液面以下 | |
| D. | 若将装置Ⅰ中Na2SO3改成NaOH溶液,现象完全相同 |
