题目内容
M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成离子化合物Z,下列说法不正确的是( )
| A、Z的熔点较高 |
| B、Z可以表示为M2Y |
| C、Z一定溶于水 |
| D、M形成+2价的阳离子 |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:元素M的两个原子失去2个电子并转移到元素Y的两个原子上,形成化合物Z,Z为离子化合物,根据原子守恒确定Z的化学式为MY2,结合离子化合物的性质解答该题.
解答:
解:A.Z为离子化合物,熔点较高,故A正确;
B.M元素的一个原子失去两个电子并转移到Y元素的两个原子中,M形成阳离子,Y形成阴离子,Z的化学式为MY2,故B错误;
C.Z为离子化合物,不一定溶于水,如CaF2,故C错误;
D.M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成+2价的阳离子,故D正确.
故选BC.
B.M元素的一个原子失去两个电子并转移到Y元素的两个原子中,M形成阳离子,Y形成阴离子,Z的化学式为MY2,故B错误;
C.Z为离子化合物,不一定溶于水,如CaF2,故C错误;
D.M元素的一个原子失去两个电子并转移到Y元素的两个原子中,形成+2价的阳离子,故D正确.
故选BC.
点评:本题考查了原子结构和元素的性质,根据得失电子确定化学键类型,再结合原子结构、物质构成分析解答,题目难度不大.

练习册系列答案
相关题目
在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气.下列说法正确的是( )
| A、乙烧杯中放入锌的质量比甲烧杯中放入锌的质量大 |
| B、甲烧杯中的酸过量 |
| C、两烧杯中参加反应的锌等量 |
| D、反应开始后乙烧杯中的c(H+ )始终比甲烧杯中的c(H+)小 |
电子数相同的两种粒子我们称二者为等电子体.如Na+和NH4+均为10电子粒子.下列物质中,不属于C3O2的等电子体的是( )
| A、N5+ |
| B、C2NO2+ |
| C、NCN2O |
| D、NC3O- |
下列实验操作中正确的是( )
| A、用干燥的pH试纸测定某氯水的pH |
| B、做完银镜反应的试管可以用氨水来洗涤 |
| C、为了除去乙酸乙酯中混有的少量乙酸,加入足量氢氧化钠溶液,充分搅拌后分液 |
| D、如果苯酚浓溶液沾到皮肤上,应立即用酒精擦洗 |
下列叙述正确的是( )
| A、可用浓硝酸除去铝制品表面的铜镀层 | ||
B、用催化法处理汽车尾气中的CO和NO:CO+NO
| ||
| C、浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体 | ||
| D、因为浓硫酸在常温下不可与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸 |
若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、在25℃,1.01×l05Pa下,1.12L O2含有的分子数是0.05NA |
| B、在25℃,1.01×106Pa下,0.1mol N2含有的原子数是0.2NA |
| C、在同温同压下,同体积任何气体所含原子数相同 |
| D、在同温同压下,两种气体的密度比等于质量之比 |
下列说法错误的是( )
| A、下列仪器中①漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥滴定管;⑦燃 烧 匙,常用于物质分离的是①③⑤ |
| B、甲酸溶液滴到大理石台板上有气泡产生:2H++CaCO3═CO2↑+Ca2++H2O |
| C、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉溶解 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量不相等 |
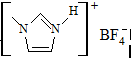 的熔点(填>、=或<),其原因是
的熔点(填>、=或<),其原因是