题目内容
13.2008年9月份,国家质检总局调查结果显示:三鹿牌婴幼儿配方奶粉是被三聚氰胺所污染,它可由三聚氰酸[C3N3(OH)3]制备.三聚氰酸可用于消除汽车尾气中的NO2,已知三聚氰酸中氮元素的化合价为-3价,有关反应原理为:①C3N3(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$3HCNO;②8HCNO+6NO2$\frac{\underline{\;\;△\;\;}}{\;}$7N2+8CO2+4H2O下列说法正确的是( )| A. | 反应①中的两种物质互为同素异形体 | |
| B. | 反应②中HCNO是氧化剂 | |
| C. | 反应②中N2既是氧化产物,又是还原产物 | |
| D. | 反应②中NO2是还原剂 |
分析 A.同种元素的不同单质是同素异形体,根据物质的组成元素种类判断;
B.得电子化合价降低的反应物是氧化剂;
C.反应中只有N元素的化合价变化;
D.失电子化合价升高的反应物是还原剂.
解答 解:A.C3N3(OH)3和HCNO是化合物不是单质,所以不是同素异形体,故A错误;
B.反应②中HCNO失电子是还原剂,故B错误;
C.反应中只有N元素的化合价变化,则生成的N2既是氧化产物,又是还原产物,故C正确;
D.反应②中NO2得电子是氧化剂,故D错误;
故选C.
点评 本题考查基本概念的判断、转移电子数的确定等知识点,难度不大,注意同素异形体和同分异构体的区别.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
3.下列物质中能通过化合反应制取的是( )
①Fe3O4 ②Fe(OH)3 ③FeCl2 ④FeCl3.
①Fe3O4 ②Fe(OH)3 ③FeCl2 ④FeCl3.
| A. | ①④ | B. | ①②④ | C. | ①③④ | D. | ①②③④ |
4.汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.8kJ•mol-1,在一容积为5L的恒容密闭容器中充人0.2mol NO和0.5mol CO,5min后该反应达到平衡,此时N2的物质的量为0.06mol.下列说法正确的是( )
| A. | 达到平衡后,若只升高温度,化学平衡正向移动 | |
| B. | 达到平衡后,再通入稀有气体,逆反应速率增大 | |
| C. | 使用催化剂,平衡常数不变 | |
| D. | 0~5 min内,NO的反应速率为2.4×1 0-3 mol•L-1•min-1 |
2.甲基丙烯酸羟乙脂(用M表示)是有机合成中的一种重要原料.其结构简式为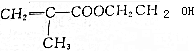 ,下列说法错误的是( )
,下列说法错误的是( )
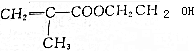 ,下列说法错误的是( )
,下列说法错误的是( )| A. | M能发生加成反应 | |
| B. | M能发生取代反应 | |
| C. | 一定条件下,M能与乙醇发生酯化反应 | |
| D. | M既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
5.在含有大量的Fe3+、Cl-、SO42-的溶液中还可能大量存在的离子是( )
| A. | Ag+ | B. | H+ | C. | OH- | D. | Ba2+ |
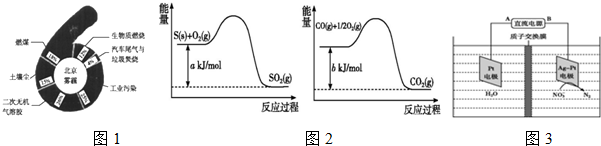
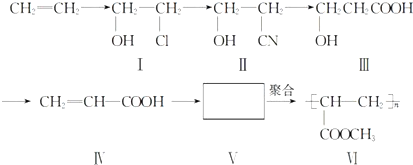
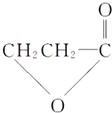 .(提示:该反应的逆反应原子利用率为100%)
.(提示:该反应的逆反应原子利用率为100%)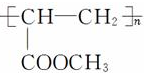 ;
;