题目内容
16.120℃时,1L气态烃在5L的氧气中完全燃烧,反应后气体体积变为6.5L(温度和压强均不变),则该烃不可能是( )| A. | 丙烷 | B. | 丙烯 | C. | 1,3-丁二烯 | D. | 乙烷 |
分析 120℃时水为气态,设该烃的化学式为CxHy,反应前后的温度压强不变,则反应后体积变化=6.5L-(1+5)L=0.5L,结合反应的化学方程式CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O利用差量法讨论;注意对于1,3丁二烯,氧气不足,反应反应为C4H6+5O2$\stackrel{点燃}{→}$CO+3CO2+3H2O,需要另外分析.
解答 解:设该烃的化学式为CxHy,该烃燃烧的化学方程式为:CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,
反应前后的温度压强不变,则容器容积与气体体积成正比,120℃时水为气态,反应后气体体积增加了:6.5L-(1+5)L=0.5L,
1L丙烷、丙烯、乙烷完全反应消耗的体积小于5L,而1L1,3-丁二烯完全燃烧消耗的氧气为5.5L,说明氧气不足,
①对于丙烷、丙烯、乙烷,烃都能够完全燃烧,则
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O△V
1 $\frac{y}{4}$-1
1L 0.5L
$\frac{y}{4}$-1=0.5,解得y=6,即烃分子中含有6个H原子,可能为丙烯、乙烷,不可能为丙烷;
②对于1,3-丁二烯,反应产物为CO、二氧化碳的化合物,烃和氧气的物质的量之比为1:5,发生反应为:C4H6+5O2$\stackrel{点燃}{→}$CO+3CO2+3H2O,1L1,3-丁二烯完全反应后体积变为1L+3L+3L=7L≠6.5L,不满足条件,
故选AC.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应实质为解答关键,注意掌握讨论法、差量法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

| A. | 金不溶于任何溶液 | |
| B. | 铜、锌在空气中均能被氧化成对应的氧化物 | |
| C. | 铜锌合金的熔点低于铜或锌的熔点 | |
| D. | ${\;}_{29}^{63}$Cu的质子数和中子数之差为34 |
| A. | 将食物储存在冰箱里 | |
| B. | 用块状碳酸钙代替粉末状碳酸钙与稀盐酸反应 | |
| C. | 往H2O2溶液中加入几滴FeCl3溶液 | |
| D. | 用纯锌代替粗锌与1 mol/L H2SO4溶液反应 |
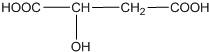 近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )
近年来流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸是这种饮料的主要酸性物质,苹果酸的结构如图所示,下列相关说法不正确的是( )| A. | 苹果酸在一定条件下能发生酯化反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 苹果酸在一定条件下能发生消去反应 | |
| D. | 1mol苹果酸与金属钠作用,最多能产生3mol氢气 |
| A. | 在H202分解中加入MnO2 | |
| B. | Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 | |
| C. | 在NaOH与HCL两溶液反应时,增大压强 | |
| D. | Na与水反应时增大水的用量 |
| A. | (0.05+a) mol | B. | 0.5a mol | C. | 0.1a mol | D. | 2a mol |
| A. | 1 mol H2O的质量为18g/mol | B. | 3.01×1023个SO2分子的质量为32g | ||
| C. | CH4的摩尔质量为16g | D. | 44g CO2含有的O原子数为NA |
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一等容的密闭容器中,用气体传感器测得了不同时间的NO和CO的浓度如表(CO2和N2的起始浓度为0).
| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (×10-4,mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO) (×10-3,mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
(1)已知在上述反应中,反应物总能量大于生成物总能量,则正反应是放热反应(填“放热”或“吸热”).
(2)前3s内的平均反应速率:υ(N2)=1.42×10-4mol/(L•s).
(3)t1℃时该反应的平衡常数表达式:K=$\frac{{c}^{2}(C{O}_{2})×c({N}_{2})}{{c}^{2}(NO)×{c}^{2}(CO)}$.
(4)假设在密闭容器中该反应达到平衡后,改变下列条件,能提高NO转化率的是cd(选填答案编号).
a.选用更有效的催化剂 b.升高反应体系的温度
c.降低反应体系的温度 d.缩小容器的体积.
