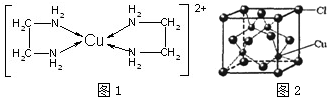
��Ŀ����
11�� ��ȩ��֬��phenolic resin��������ϳɵĵ�һ�ָ߷��Ӳ��ϣ������Ա��㷺ʹ�ã�ijУ��ѧ��ȤС���ͬѧͨ�����з�����ʵ�����Ʊ���ȩ��֬��
��ȩ��֬��phenolic resin��������ϳɵĵ�һ�ָ߷��Ӳ��ϣ������Ա��㷺ʹ�ã�ijУ��ѧ��ȤС���ͬѧͨ�����з�����ʵ�����Ʊ���ȩ��֬�����ȡ50.0 g���Ӿ�������һ���Թ��У����ڴ��Թܼ���35.4 mL 40%�ĸ���������Һ���ܶȣ�1.06 g/mL��������Ũ���ᣮ
���������Թ���������ͼ��ʾ��װ�ã���ˮ����30��45min��
���Թ������ɵİ�ɫ�Դ���ɫ����֬ȫ��ȡ����������ˮϴ��5���Ӻ����ɡ����أ������ͷ�ȩ��֬50.0 g��
��ش��������⣺
��1��д���ϳɷ�ȩ��֬�Ļ�ѧ����ʽ
 ��
����2�������ڳ���������ɫ���壬���״��Լ�ƿ��ȡ����ʵ��ʱ�ɲ�ȡ�ò��������Լ�ƿ�б��Ӿ������ᵷ�飬����ҩ��ȡ�������Ȱ�װ�б��ӵ��Լ�ƿ����60��70�����ˮ�У�ʹ�����ڻ������ó��ι��������ķ���ȡ�����ӣ�ȡ�ñ���ʱ����С�Ľ�����մ��Ƥ���ϣ�Ӧ��ȡ�Ĵ�ʩ�������þƾ���ϴ�ɾ���
��3����ʵ�������õļ��ȷ�����Ϊˮԡ���ȣ�����ʵ���⣬���پٳ�һ�����ø÷������ȵ�ʵ��������Ӧ��
��4��װ���г����ܵ�������������������߷�Ӧ���ʣ�
��5�������ķ�ȩ��֬Ϊ��ɫ���壬����ʵ���еõ��ķ�ȩ��֬�Դ���ɫ��ԭ����δ��Ӧ�ı��ӱ�����������ʵ���������ϴ���Թܵķ����Ǽ����������Ҵ����ݼ����Ӻ�����ϴ��
��6����ʵ���з�ȩ��֬�IJ���Ϊ94.3%��
���� ��1�����Ӻͼ�ȩ��ˮԡ���ȵ��������������۷�Ӧ���ɷ�ȩ��֬��
��2�����Լ�ƿ��ȡ��ȡ�����ӣ����Խ��������ᵷ��Ҳ���Է���ˮԡ�м����ۻ������ó��ι����������ڱ��������ھƾ������Կ����þƾ���ȥƤ���ϵı��ӣ�
��3������ʵ��װ��ͼ��֪��ʵ�������õļ��ȷ�����Ϊˮԡ���ȣ�һ������¶Ȳ�����100��ʱ��������ˮԡ���ȣ�
��4�����Ӻͼ�ȩ�����ӷ��Ե����ʣ�Ϊ����߷�Ӧ���ʵ�ת���ʣ�Ҫ����Ӧ������������
��5�������ױ������ʺ�ɫ����ȩ��֬Ҫ�þƾ���������ϴ��
��6��50.0 g���ӵ����ʵ���Ϊ$\frac{50}{94}$mol=0.532mol��35.4 mL 40%�ĸ���������Һ�м�ȩ�����ʵ���Ϊ$\frac{35.4��1.06��40%}{30}$mol=0.5mol�����Ӻͼ�ȩ��1��1��Ӧ���ɷ�ȩ��֬���������ɷ�ȩ��֬�����ʵ���Ϊ0.5mol�����ݲ���=$\frac{ʵ�ʲ���}{���۲���}$��100%���㣮
��� �⣺��1�����Ӻͼ�ȩ��ˮԡ���ȵ��������������۷�Ӧ���ɷ�ȩ��֬����Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��2�����Լ�ƿ��ȡ��ȡ�����ӣ����Խ��������ᵷ��Ҳ���Է���ˮԡ�м����ۻ������ó��ι����������ڱ��������ھƾ������Կ����þƾ���ȥƤ���ϵı��ӣ�
�ʴ�ΪΪ���ò��������Լ�ƿ�б��Ӿ������ᵷ�飬����ҩ��ȡ�������Ȱ�װ�б��ӵ��Լ�ƿ����60��70�����ˮ�У�ʹ�����ڻ������ó��ι��������������þƾ���ϴ�ɾ���
��3������ʵ��װ��ͼ��֪��ʵ�������õļ��ȷ�����Ϊˮԡ���ȣ�һ������¶Ȳ�����100��ʱ��������ˮԡ���ȣ�����������Ӧ�ȣ�
�ʴ�Ϊ��ˮԡ���ȣ�������Ӧ��
��4�����Ӻͼ�ȩ�����ӷ��Ե����ʣ�Ϊ����߷�Ӧ���ʵ�ת���ʣ�Ҫ����Ӧ����������������װ���г����ܵ�������������������߷�Ӧ���ʣ�
�ʴ�Ϊ��������������߷�Ӧ���ʣ�
��5��ʵ���еõ��ķ�ȩ��֬�Դ���ɫ������Ϊδ��Ӧ�ı��ӱ������ʺ�ɫ����ϴ���Թ��еķ�ȩ��֬Ҫ�þƾ���������ϴ��
�ʴ�Ϊ��δ��Ӧ�ı��ӱ����������� �����������Ҵ����ݼ����Ӻ�����ϴ��
��6��50.0 g���ӵ����ʵ���Ϊ$\frac{50}{94}$mol=0.532mol��35.4 mL 40%�ĸ���������Һ�м�ȩ�����ʵ���Ϊ$\frac{35.4��1.06��40%}{30}$mol=0.5mol�����Ӻͼ�ȩ��1��1��Ӧ���ɷ�ȩ��֬���������ɷ�ȩ��֬�����ʵ���Ϊ0.5mol��������Ϊ53g�����Բ���=$\frac{ʵ�ʲ���}{���۲���}$��100%=$\frac{50g}{53g}$��100%=94.3%��
�ʴ�Ϊ��94.3%��
���� ���⿼��ѧ����ȩ��֬���й�֪ʶ��Ҫ��ѧ����Ϥ�α����ݣ�������ѧ֪ʶ���ش��ѶȲ���

| A�� | HCl��Na2CO3��HNO3��KHCO3 | B�� | BaCl2��Na2SO4��Ba��OH��2��CuSO4 | ||
| C�� | HCl��KOH��H2SO4��Ba��OH��2 | D�� | H2SO4��NaHCO3��NaHSO4��KHCO3 |
�ٵ��������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
2NO2��g��+NaCl��s��?NaNO3��s��+ClNO��g����H1 K1
4NO2��g��+2NaCl��s��?2NaNO3��s��+2NO��g��+Cl2��g����H2 K2
2NO��g��+Cl2��g��?2ClNO��g����H3 K3
���H3=2��H1-��H2���á�H1�͡�H2��ʾ����K3=$\frac{K_1^2}{K_2}$����K1��K2��ʾ����
��NaOH��Һ�������յ��������NO2+NO+2NaOH=2NaNO2+H2O�������£���һ������NaOH
��Һ����NO��NO2������壬�õ�0.1mol/L��NaNO2��Һ����֪HNO2�ĵ��볣��Ka=7.1��10-4��
��ô������NO2-��ˮ�ⳣ��Kh=1.4��10-11��0.1mol/L NaNO2��Һ�д�c��Na+ ����c��OH- ����c��NO2- ����c��HNO2���Ĵ�С˳��Ϊc��Na+ ����c��NO2-����c��OH-����c��HNO2����
��2����3.0L�ܱ������У�ͨ��0.10mol CH4��0.20mol NO2����һ���¶��½��з�Ӧ��CH4��g��+2NO2��g��?CO2��g��+N2��g��+2H2O��g����H��0����Ӧʱ�䣨t����������������ѹǿ��p�������ݼ��±���
| ʱ��t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| ��ѹǿp/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
����һ����װ���У�ͨ��һ����CH4��NO2���������ͬʱ���ڣ��ڲ�ͬ�¶��£�NO2��ת������ͼ��������Ϊ��Ӧ�¶ȣ�������ΪNO2ת����/%����

������������ȷ����AD��
A�����¶�ά����200�����ʱ�䣬NO2��ת���ʽ�����19%
B����Ӧ���ʣ�b���v ���棩��e��� v ���棩
C��ƽ�ⳣ����c��=d��
D�����b��ʱNO2��ת���ʺͷ�Ӧ���ʣ����ʵ����»�����c��CH4��
 ��1�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ[��Ӧ��O2��g����������H2O��g����ȥ]��
��1�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ[��Ӧ��O2��g����������H2O��g����ȥ]�������д��������£�CH3OH��O2��Ӧ��Ҫ����HCHO���CO��CO2����HCHO������2HCHO��g��+O2��g��=2CO��g��+2H2O��g����H=-470KJ•mol-1��
�ڼ״���ȡ��ȩ����Ag������������AgCl�� Ӱ��Ag�����Ļ��ԣ��ð�ˮ�����ܽ��ȥ���е�AgCl��д���÷�Ӧ�����ӷ���ʽ��AgCl+2NH3•H2O=Ag��NH3��2++Cl-+2H2O��AgCl+2NH3=Ag��NH3��2++Cl-��
��2����֪��CO��g��+2H2��g��?CH3OH��g����H��0CH3OH��g����H=-a kJ•mol-1��
�پ��ⶨ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����£�
| �¶ȣ��棩 | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
��ij�¶��£�������̶���2L���ܱ������н�1mol CO��2mol H2��ϣ���ò�ͬʱ�̵ķ�Ӧǰ��ѹǿ��ϵ���£�
| ʱ�䣨min�� | 5 | 10 | 15 | 20 | 25 | 30 |
| ѹǿ�ȣ�P��/Pǰ�� | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
��3�������Ƽ�ѭ�����ɳ�ȥSO2������SO2�Ի�������Ⱦ������Һ����SO2�Ĺ����У�pH��n��SO32-����n��HSO3-���仯��ϵ���±���
| n��SO32-����n��HSO3-�� | 91��9 | 1��1 | 1��91 |
| pH | 8.2 | 7.2 | 6.2 |
����NaHSO3��Һ������Ũ�ȹ�ϵ��ȷ����ac ������ĸ����
a��c��Na+����c��HSO3-����c��H+����c��SO32-����c��OH-��
b��c��Na+��=2c��SO32-��+c��HSO3-��
c��c��H2SO3��+c��H+��=c��SO32-��+��OH-��
d��c�� Na+��+c��H+��=c��SO32-��+c��HSO3-��+c��OH-��
| A�� |  ��ͼ��ʾ���ⶨ�кͷ�Ӧ�ķ�Ӧ��ʱ����С���ձ�����������ĭ���ϵ������ǹ̶�С�ձ� ��ͼ��ʾ���ⶨ�кͷ�Ӧ�ķ�Ӧ��ʱ����С���ձ�����������ĭ���ϵ������ǹ̶�С�ձ� | |
| B�� | ����50 mL 0.55 mol•L-1������������Һ���ֱ���50 mL 0.50 mol•L-1�������50 mLA0.50 mol•L-1�������ַ�Ӧ������Ӧ�ⶨ�ķ�Ӧ�Ȳ���� | |
| C�� | ʵ��ʱ��Ҫ��¼��ʼ�¶�T1 ������¶�T2 | |
| D�� | ��һ��ʵ����ݹ�ʽ���ɵó��кͷ�Ӧ�ķ�Ӧ�� |
��1��ʵ�����ϱ����ձ�����С�����ձ�������ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β����������0.5mol•L-1 ���ᡢ0.55mol•L-1NaOH��Һ����ȱ�ٵ�ʵ�鲣����Ʒ����Ͳ���¶ȼƣ�
��2��ʵ�����ܷ��û���ͭ˿��������滷�β��������������ܡ�������ԭ����ͭ˿���������ã�����к��ȵļ������Ӱ�죮
��3�����Ǽ�¼��ʵ���������£�
| ʵ �� �� Ʒ | �� Һ �� �� | �к��� ��H | |||
| t1 | t2 | ||||
| �� | 50mL 0.55mol��L-1NaOH | 50mL 0.5mol��L-1HCl | 20�� | 23.3�� | |
| �� | 50mL 0.55mol��L-1NaOH | 50mL 0.5mol��L-1HCl | 20�� | 23.5�� | |
��4������KOH����NaOH���Բⶨ����ޣ���С����ޡ���Ӱ�죮

| A�� | 2SO3��g��?2SO2��g��+O2��g����H��0 | B�� | N2��g��+3H2��g��?2NH3��g����H��0 | ||
| C�� | 4NH3��g��+5O2��g��?4NO+6H2O��g����H��0 | D�� | H2��g��+CO��g��?C��s��+H2O��g����H��0 |