题目内容
13.氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2.某同学在实验室中对NH3与NO2反应进行了探究.回答下列问题:(1)氨气的制备
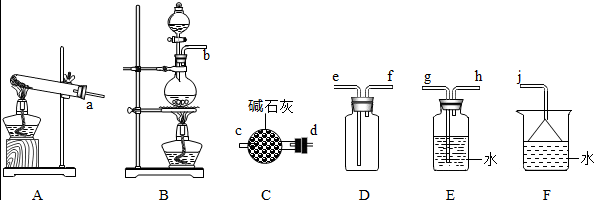
①氨气的发生装置可以选择上图中的A,反应的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→d→c→f→e→j(按气流方向,用小写字母表示).
(2)氨气与二氧化氮的反应
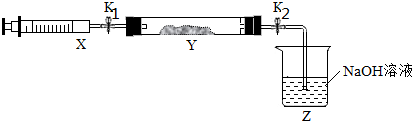
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度下按图示装置进行实验.
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中红棕色气体慢慢变浅 | ②反应的化学方程式 8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | ③Z中NaOH溶液产生倒吸现象 | ④反应后气体分子数减少,Y管压强小于外压 |
分析 (1)①实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,依据反应物状态和条件选择发生装置;
②气体制备一般顺序为:发生装置,净化装置,收集装置,尾气处理装置,结合氨气为碱性气体,密度小于空气密度,极易溶于水的性质解答;
(2)打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中,则氨气与二氧化氮发生归中反应生成无色氮气,所以看到现象为:红棕色变浅;
依据8NH3+6NO2=7N2+12H2O以及气态水凝聚判断反应后气体分子数减少从而判断打开K2发生的现象.
解答 解:(1)①实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,反应物状态为固体与固体,反应条件为加热,所以选择A为发生装置,反应方程式:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
故答案为:A;Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②实验室用加热固体氯化铵和氢氧化钙的方法制备氨气,制备的气体中含有水蒸气,氨气为碱性气体,应选择盛有碱石灰干燥管干燥气体,氨气极易溶于水,密度小于空气密度所以应选择向下排空气法收集气体,氨气极易溶于水,尾气可以用水吸收,注意防止倒吸的发生,所以正确的连接顺序为:发生装置→d→c→f→e→j;
故答案为:d→c→f→e→j;
(2)打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中,则氨气与二氧化氮发生归中反应 生成无色氮气,所以看到现象为:红棕色气体慢慢变浅;
根据反应8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O以及装置恢复至室温后气态水凝聚可判断反应后气体分子数减少,装置内压强降低,所以打开K2在大气压的作用下发生倒吸;
故答案为:
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①红棕色气体慢慢变浅 | ②反应的化学方程式 8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | ③Z中NaOH溶液产生倒吸现象 | ④反应后气体分子数减少,Y管中压强小于外压 |
点评 本题考查了氨气的制备和性质的检验,明确氨气的制备原理及制备气体的一般程序是解题关键,题目难度不大.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案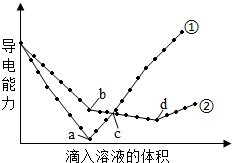 在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )| A. | ①代表滴加H2SO4溶液的变化曲线 | |
| B. | b点,溶液中大量存在的离子是Na+、OH- | |
| C. | c点,两溶液中含有相同量的OH- | |
| D. | a、d两点对应的溶液均显中性 |
又有利于资源综合利用.废钒催化剂的主要成分为:
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
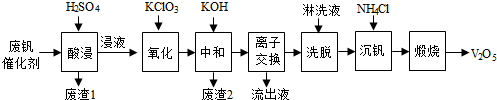
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为V2O5+2H+=2VO2++H2O,同时V2O4转成VO2+.“废渣1”的主要成分是SiO2.
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为0.5mol.
(3)“中和”作用之一是使钒以V4O124-形式存在于溶液中.“废渣2”中含有Fe(OH)3、Al(OH)3.
(4)“离子交换”和“洗脱”可简单表示为:4ROH+V4O124-$?_{洗脱}^{离子交换}$R4V4O12+4OH-(以ROH为强碱性阴离子交换树脂).为了提高洗脱效率,淋洗液应该呈碱性(填“酸”“碱”“中”).
(5)“流出液”中阳离子最多的是K+.
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式2NH4VO3$\frac{\underline{\;高温\;}}{\;}$V2O5+H2O↑+2NH3↑.
| A. | 1:1 | B. | n:(n+1) | C. | 1:(n+1) | D. | (n+1):n |
| A. | 该醇至少含有两个碳原子 | B. | 该醇分子中一定没有甲基 | ||
| C. | 该醇分子中一定含有甲基 | D. | 该醇分子中含有一个醇羟基 |
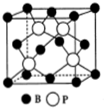 氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.