题目内容
下列溶液中Cl-浓度最小的是( )
| A、200mL 2mol/L MgCl2溶液 |
| B、500mL 2mol/L NaCl溶液 |
| C、300mL 5mol/L KCl溶液 |
| D、400mL 1mol/L AlCl3溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:电解质离子浓度=电解质浓度×电解质电离出的该离子数目,与溶液的体积无关,据此结合选项计算判断.
解答:
解:A、200mL 2mol/L MgCl2溶液中c(Cl-)=2mol/L×2=4mol/L;
B、500mL 2mol/L NaCl溶液中c(Cl-)=2mol/L×1=2mol/L;
C、300mL 5mol/L KCl溶液中c(Cl-)=5mol/L×1=5mol/L;
D、400mL 1mol/L AlCl3溶液中c(Cl-)=1mol/L×3=3mol/L;
故500mL 2mol/L NaCl溶液中Cl-浓度最小,
故选B.
B、500mL 2mol/L NaCl溶液中c(Cl-)=2mol/L×1=2mol/L;
C、300mL 5mol/L KCl溶液中c(Cl-)=5mol/L×1=5mol/L;
D、400mL 1mol/L AlCl3溶液中c(Cl-)=1mol/L×3=3mol/L;
故500mL 2mol/L NaCl溶液中Cl-浓度最小,
故选B.
点评:本题考查离子物质的量浓度的有关计算,难度不大,注意电解质离子浓度与电解质浓度关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质都是还原剂的是( )
| A、H+、S、K+、Cl2 |
| B、Fe2+、Zn、S2-、C |
| C、Fe3+、I-、H2、CO |
| D、Al、Zn2+、Na、I- |
下列粒子结构示意图中,表示阴离子的是( )
A、 |
B、 |
C、 |
D、 |
下列各表述与示意图一致的是
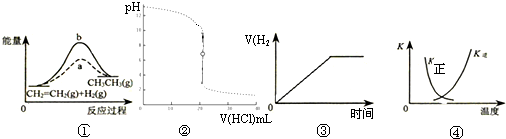

| A、图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)+Q使用和未使用催化剂时,反应过程中的能量变化 |
| B、图②表示25℃时,用0.1mol?L-1盐酸滴定20mL 0.1mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| C、图③表示锌粒与过量稀盐酸反应时,V(H2) 随时间的变化图 |
| D、图④中曲线表示反应2SO2(g)+O2(g)=2SO3(g)+Q 正、逆反应的平衡常数K随温度的变化 |
下列有关说法中正确的是( )
| A、由氧化物组成的分子有Na2O?Al2O3?2SiO2?nH2O,可用于分离、提纯气体及作干燥剂、离子交换剂、催化剂及催化剂载体等 |
| B、大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 |
| C、聚氯乙烯中的氯元素可以用铜丝燃烧法、钠熔法、质谱法、红外光谱法等方法进行检测 |
| D、工业上可以NaOH溶液、CS2溶液棉短绒、木浆中的纤维素,再压入酸中得到人造棉、人造丝等合成纤维 |
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、23g金属钠变为钠离子时失去的电子数为NA |
| B、标准状况下,18g水所含的氢原子数目为2NA |
| C、标准状况下,22.4 L氦气所含的原子数目为2NA |
| D、1mol?L-1 CuCl2溶液中含氯离子数为0.2NA |
Cu、Cu2O和CuO组成的混合物,加入100mL 0.6mol/LHNO3溶液恰好使混合物溶解,同时收集到224mLNO气体(标准状况).下列说法不正确的是( )
| A、产物中硝酸铜的物质的量为0.025 mol |
| B、若混合物中Cu的物质的量为x,则其中Cu2O、CuO的物质的量共0.020 mol |
| C、若混合物中含0.01moLCu,则其中Cu2O、CuO的物质的量均为0.005 mol |
| D、混合物中Cu的物质的量的取值范围为0.005mol<n(Cu)<0.015mol |