题目内容
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、23g金属钠变为钠离子时失去的电子数为NA |
| B、标准状况下,18g水所含的氢原子数目为2NA |
| C、标准状况下,22.4 L氦气所含的原子数目为2NA |
| D、1mol?L-1 CuCl2溶液中含氯离子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,结合钠原子最外层的电子数为1计算分析;
B、依据n=
计算物质的量,结合分子式计算原子数;
C、依据n=
计算物质的量,氦气是单原子分子;
D、溶液体积不知不能计算微粒数;
| m |
| M |
B、依据n=
| m |
| M |
C、依据n=
| V |
| Vm |
D、溶液体积不知不能计算微粒数;
解答:
解:A、依据n=
计算物质的量=
=1mol,结合钠原子最外层的电子数为1计算分析变为钠离子时失去的电子数为NA,故A正确;
B、依据n=
计算物质的量=
=1mol,18g水所含的氢原子数目为2NA,故B正确;
C、依据n=
计算物质的量=
=1mol,氦气是单原子分子,22.4 L氦气所含的原子数目为NA,故C错误;
D、溶液体积不知不能计算微粒数,故D错误;
故选AB.
| m |
| M |
| 23g |
| 23g/mol |
B、依据n=
| m |
| M |
| 18g |
| 18g/mol |
C、依据n=
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
D、溶液体积不知不能计算微粒数,故D错误;
故选AB.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是微粒结构和微粒数目计算应用,注意氦气是单原子分子,题目较简单.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、过氧化钠和冷水反应:Na2O2+H2O═2Na++2OH-+H2↑ |
| B、NaHCO3溶于氢氧化钠溶液:HCO3-+OH-=H2O+CO2↑ |
| C、金属铝溶于稀硫酸中:2Al+6H+═2Al3++3H2↑ |
| D、铜跟稀硫酸反应:Cu+2H+═Cu2++H2↑ |
下列实验与对应示意图的关系正确的是( )
A、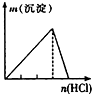 NaAlO2溶液中逐滴滴加稀盐酸至过量 |
B、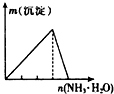 AlCl3溶液中逐滴滴加氨水至过量 |
C、 明矾溶液中逐滴滴加Ba(OH)2至过量 |
D、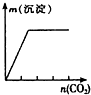 澄清石灰水中缓慢通入CO2至过量 |
下列溶液中Cl-浓度最小的是( )
| A、200mL 2mol/L MgCl2溶液 |
| B、500mL 2mol/L NaCl溶液 |
| C、300mL 5mol/L KCl溶液 |
| D、400mL 1mol/L AlCl3溶液 |
 硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( )
硝酸钾和氯化钾的溶解度曲线如图所示,下列叙述正确的是( )| A、硝酸钾的溶解度一定大于氯化钾的溶解度 |
| B、降低温度可使接近饱和的硝酸钾溶液变饱和 |
| C、t℃时,硝酸钾和氯化钾两种溶液的溶质质量分数一定相等 |
| D、60℃时,100 g水中加入90 g硝酸钾,充分搅拌,可得到硝酸钾的饱和溶液 |
下列叙述中,正确的是( )
| A、放热反应均能自发进行 |
| B、化学平衡发生移动,平衡常数必发生变化 |
| C、某特定反应的平衡常数仅是温度的函数 |
| D、△S为正值的反应均是自发进行的反应 |
下列有关“焰色反应”说法中正确的是( )
| A、非金属单质燃烧时火焰均为无色 |
| B、所有金属及其化合物灼烧时火焰均有颜色 |
| C、NaCl与Na2CO3灼烧时火焰颜色相同 |
| D、焰色反应均应透过蓝色钴玻璃观察 |
以下关于化学实验中“先与后”的说法中正确的是( )
| A、加热试管时,先均匀加热,后集中加热 |
| B、用排水法收集气体后,先撤酒精灯后移出导管 |
| C、制取气体时,先装药品后检验装置气密性 |
| D、称量NaOH固体时,先在托盘上各放两张完全相同的纸,再加药品 |
瓦斯中甲烷与氧气的质量比为1:4极易爆炸,此时氧气和甲烷的体积比为( )
| A、1:4 | B、1:2 |
| C、1:1 | D、2:1 |