题目内容
12.下列有关金属的工业制法中,正确的是( )| A. | 制铝:以铝土矿为原料获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 | |
| B. | 制镁:用海水为原料,经一系列过程制得氧化镁固体,电解熔融氧化镁得镁 | |
| C. | 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 | |
| D. | 制铁:以铁矿石为原料,利用焦炭与氧气反应生成的CO在高温下还原得铁 |
分析 A.AlCl3为共价键化合物,熔融AlCl3中没有离子,不能导电;
B.海水中含氯化镁,可用于工业制镁,工业制镁是电解熔融氯化镁来制取;
C.工业制钠是电解熔融NaCl来制取,电解纯净的NaCl溶液得到的是氢氧化钠和氢气和氯气;
D.工业上常用用CO在高温下还原铁矿石炼铁.
解答 解:A.因为氯化铝是分子晶体,熔融状态下氯化铝不导电,制铝:从铝土矿中获得氧化铝再电解熔融的氧化铝来获取金属铝,故A错误;
B.镁和热水反应生成氢氧化镁和氢气,不能用氢气还原氧化镁制取镁,工业制镁是电解熔融氯化镁:MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑,故B错误;
C.工业制钠是电解熔融NaCl:2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑,而电解纯净的NaCl溶液:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,得不到钠,故C错误;
D.工业上常用用CO在高温下还原铁矿石炼铁:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,制得铁,故D正确;
故选D.
点评 本题主要考查了有关金属的工业制法,掌握钠、铁、镁、铝及其化合物的性质是解答的关键,题目难度不大.注意氯化铝中没有自由移动的离子,是分子晶体.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
2.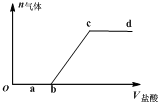 向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图.则下列离子组在对应的溶液中一定能大量共存的是( )
 向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应溶液中:Ca2+、Mg2+、Br-、NO3- | |
| B. | b点对应溶液中:Al3+、Fe3+、MnO4-、NO3- | |
| C. | c点对应溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应溶液中:F-、NO3-、Fe2+、Ag+ |
3.将N2、H2的混合气体分别充入甲、乙、丙三个容器后,测得化学反应速率分别为甲:v(H2)=3mol/(L•min);乙:v(N2)=2mol/(L•min);丙:v(NH3)=1mol/(L•S).则三个容器中合成氨的反应速率( )
| A. | v(甲)>v(乙)>v(丙) | B. | v(乙)>v(丙)>v(甲) | C. | v(丙)>v(乙)>v(甲) | D. | v(乙)>v(甲)>v(丙) |
20.据报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程如图:下列说法中不正确的是( )
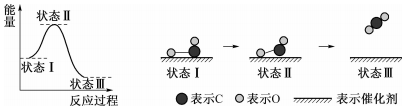

| A. | 状态Ⅰ→状态Ⅲ是放热过程 | |
| B. | 该过程中,CO没有断键形成C和O | |
| C. | 状态Ⅰ→状态Ⅲ表示CO和O生成了CO2 | |
| D. | 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 |
17.下列有机物中属于醇的是( )
| A. | 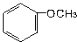 | B. | 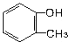 | C. | 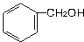 | D. | CH3-O-CH3 |
4.下列有关化学用语表示正确的是( )
| A. | 熔融状态下硫酸氢钾的电离方程式:KHSO4═K++H++SO42- | |
| B. | Cl-的结构示意图: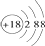 | |
| C. | 中子数为8的碳原子:${\;}_{6}^{14}$C | |
| D. | NaCl的电子式: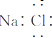 |