题目内容
10.量取10ml碘的饱和水溶液,倒入分液漏斗中,然后再注入4ml苯,用力振荡后静置,实验现象为( )| A. | 液体分层,下层为苯层,黄色 | B. | 液体分层,下层为水层,紫色 | ||
| C. | 液体分层,上层为苯层,紫色 | D. | 液体分层,上层为水层,黄色 |
分析 碘不易溶于水,易溶于苯,苯与水分层,且苯的密度比水的密度小,以此来解答.
解答 解:因碘不易溶于水,易溶于苯,苯与水分层,且苯的密度比水的密度小,则碘的饱和水溶液,倒入分液漏斗中,然后再注入苯,用力振荡后静置,实验现象为液体分层,上层为苯层,紫色,而下层为无色的水层,
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意萃取现象的判断,题目难度不大.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
5.可溶性铝盐与强碱溶液反应,铝元素的存在形式如图,则a、b的差值为( )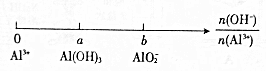
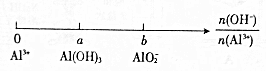
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
6.饮食合理、营养均衡是健康的基本保证.下列食物中,富含糖类的是( )
| A. | 橄榄油 | B. | 蔬菜 | C. | 米饭 | D. | 苹果 |
3.表是生活生产中常见的物质,表中列出了它们的一种主要成分(其它成分未列出)
(1)请你对表中①~⑦的主要成分进行分类(填编号)属于盐的是①③,属于电解质的是①②③⑦,属于非电解质的是④⑥.
(2)写出②与⑦反应的离子方程式CH3COOH+OH-=CH3COO-+H2O.少量盐酸与③反应的离子方程式为CO32-+H+=HCO3-.
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 绿矾 | 醋精 | 苏打 | 酒精 | 铜导线 | 蔗糖 | 烧碱 |
| 主要成分 | FeSO4 | CH3COOH | Na2CO3 | CH3CH2OH | Cu | C12H22O11 | NaOH |
(2)写出②与⑦反应的离子方程式CH3COOH+OH-=CH3COO-+H2O.少量盐酸与③反应的离子方程式为CO32-+H+=HCO3-.
19.铋(Bi)位于元素周期表中ⅤA族,+3价较稳定,铋酸钾(KBiO3)溶液呈无色.取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如表所示:
关于KBiO3、KMnO4、I2、H2O2的氧化性由弱到强(从左至右)的顺序为( )
| 加入溶液 | ①适量的铋酸钾溶液 | ②过量的双氧水 | ③适量KI-淀粉溶液实验 |
| 现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A. | KBiO3、KMnO4、H2O2、I2 | B. | KMnO4、KBiO3、I2、H2O2 | ||
| C. | I2、H2O2、KMnO4、KBiO3 | D. | H2O2、I2、KBiO3、KMnO4 |
20.反应A+3B=2C+D在四种不同情况下的反应速率,其中最快的是( )
| A. | V(A)=0.15mol/(L•s) | B. | V(B)=0.6mol/(L•s) | C. | V(C)=0.5mol/(L•s) | D. | V(D)=0.45mol/(L•s) |