题目内容
17. 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.利用如图装置可以验证非金属性的变化规律.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.利用如图装置可以验证非金属性的变化规律.(1)仪器A的名称为分液漏斗,干燥管D的作用是防止倒吸.
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为浓盐酸、KMnO4、Na2S,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为S2-+Cl2═S↓+2Cl-.
(3)若要证明非金属性:C>Si,则A中加入硫酸(填试剂名称)、B装置中加Na2CO3粉末、C装置中加入Na2SiO3(填试剂名称),观察到C中溶液的现象为有白色胶状沉淀产生.
分析 (1)根据仪器的构造写出仪器A的名称;球形干燥管具有防止倒吸的作用;
(2)设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证;
(3)要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明.
解答 解:(1)仪器A为分液漏斗,球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,故答案为:分液漏斗;防止倒吸;
(2)设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、KMnO4、Na2S溶液,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为S2-+Cl2═S↓+2Cl-,
故答案为:浓盐酸、KMnO4、Na2S;S2-+Cl2═S↓+2Cl-;
(3)若要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明,由于B中加Na2CO3,故A中可以加硫酸,通过硫酸和碳酸钠的反应来制取CO2,然后的CO2通入C中的Na2SiO3中,可以发生反应:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,产生白色胶状沉淀,从而可以证明酸性:H2CO3>H2SiO3,故非金属性:C>Si.
故答案为:硫酸;Na2SiO3;有白色胶状沉淀产生.
点评 本题考查了实验方案设计,涉及金属、非金属性强弱的探究,明确物质的性质是解本题关键,同时考查学生灵活运用知识解答问题的能力,题目难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
9.下列离子反应不能发生的是( )
| A. | NaOH+KCl=NaCl+KOH | B. | AgNO3+NaCl=AgCl↓+NaNO3 | ||
| C. | Na2CO3+Ca(OH)2=CaCO3↓+2NaOH | D. | NaOH+NH4NO3=NaNO3+NH3•H2O |
5.能正确表示下列反应的离子方程式是( )
| A. | 铝放入烧碱溶液中溶解:2Al+2OH-+2 H2O═2 AlO2-+3H2↑ | |
| B. | 碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 稀硫酸中加氢氧化钡溶液至中性:H++OH-═H2O | |
| D. | NaHCO3溶液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
2.在锌与盐酸反应的实验中,甲同学得到的结果如表所示:
按要求回答下列问题:
(1)温度对该反应速率的影响规律为温度越高,反应速率越快.
(2)对比结果B与F,F速率明显快的原因是粉末状的锌粉与酸接触面积大,反应速率快.
(3)乙同学将表面积相同、纯度相同、体积也相同的同种锌片分别投入等体积、浓度不同的稀硫酸和稀盐酸中(两酸中的氢离子浓度相同),仔细观察后发现,投入到稀硫酸中的锌表面产生的气泡没有投入到稀盐酸的快,产生这一现象可能的原因是:硫酸根离子可能是这一反应的负催化剂或氯离子可能是正催化剂.(只需回答一条即可)如何用实验来验证向锌和稀硫酸反应中加氯化锌若反应速率加快则证明氯离子是正催化剂,或向锌和稀盐酸反应中加硫酸锌溶液在反应中若反应速率减慢则说明硫酸根离子是负催化剂.
| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸所需的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
(1)温度对该反应速率的影响规律为温度越高,反应速率越快.
(2)对比结果B与F,F速率明显快的原因是粉末状的锌粉与酸接触面积大,反应速率快.
(3)乙同学将表面积相同、纯度相同、体积也相同的同种锌片分别投入等体积、浓度不同的稀硫酸和稀盐酸中(两酸中的氢离子浓度相同),仔细观察后发现,投入到稀硫酸中的锌表面产生的气泡没有投入到稀盐酸的快,产生这一现象可能的原因是:硫酸根离子可能是这一反应的负催化剂或氯离子可能是正催化剂.(只需回答一条即可)如何用实验来验证向锌和稀硫酸反应中加氯化锌若反应速率加快则证明氯离子是正催化剂,或向锌和稀盐酸反应中加硫酸锌溶液在反应中若反应速率减慢则说明硫酸根离子是负催化剂.
6. 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )| A. | 绿原酸分子中有4个手性碳原子(碳旁边连接4个不同的原子或原子团) | |
| B. | 绿原酸能发生显色反应、取代反应和加成反应 | |
| C. | 每摩尔绿原酸最多与4 mol NaOH反应 | |
| D. | 绿原酸分子中所有碳原子都能在同一平面上 |
7. 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )| A. | 甲一定是金属元素 | |
| B. | 气态氰化物的稳定性庚>己>戊 | |
| C. | 乙、丙、丁的最高价氧化物对应水化物可以相互反应 | |
| D. | 庚的最高价氧化物水化物酸性最强 |
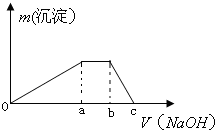 甲是一种盐,由A、B、C、D、E五种短周期元素元素组成.甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子.A元素原子核内质子数比E的少1,D、E处于同主族.用甲进行如下实验:
甲是一种盐,由A、B、C、D、E五种短周期元素元素组成.甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子.A元素原子核内质子数比E的少1,D、E处于同主族.用甲进行如下实验: