题目内容
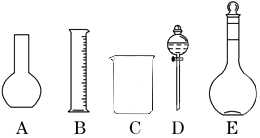
18.某学生设计了如图实验,以下说法错误的是( )
| A. | 该同学的实验目的是分离氯化钠、氯化钙 | |
| B. | 上图括号内的操作步骤均为加热蒸发 | |
| C. | 按此实验方案可得到较纯净的NaCl固体 | |
| D. | 按此实验方案可得到较纯净的CaCl2固体 |
分析 氯化钙、氯化钠的混合溶液中加入过量的碳酸钠溶液,生成白色沉淀B为碳酸钙,加入盐酸,生成C为氯化钙溶液,蒸发结晶、冷却、干燥得到氯化钙固体,加入碳酸钠后得到的旅游含有氯化钠、碳酸钠,可加入盐酸,在蒸发、结晶,得到氯化钠,以此解答该题.
解答 解:A.由以上分析可知该同学的实验目的是分离氯化钠、氯化钙,故A正确;
B.上图括号内的操作步骤用于由溶液得到晶体,则均为加热蒸发,故B正确;
C.加入过量碳酸钠,氯化钠中混有碳酸钠杂质,故C错误;
D.碳酸钙中加入盐酸,生成氯化钙,蒸干结晶得到较为纯净的氯化钙,故D正确.
故选C.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
9.二氧化硫是一种重要的化工原料,主要用于生产硫酸、亚硫酸盐等.请回答:
(1)已知2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的关键反应.如图1为不同温度(T1、T2)下SO2的转化率随时间的变化曲线.
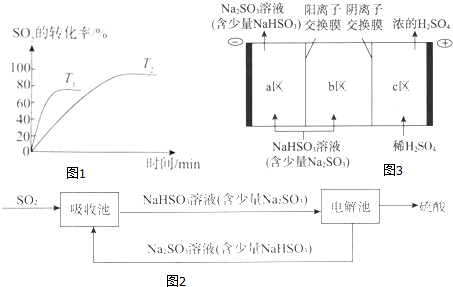
①T1>(填“>”“<”或“=”)T2,判断的依据是温度越高反应速率越快,达到化学平衡的时间越短;该反应为放(填“放”或“吸”)热反应,判断的依据是温度升高时平衡向吸热方向移动,SO2的转化率减小.
②如表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率.
i.b对应的投料比为4:15.
ii.投料比为8:10时,平衡混合气体中SO3体积分数为50%.
(2)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如图2:
①吸收池中发生反应的离子方程式是SO2+SO32-+H2O=2HSO3-.
②电解池的构造示意图如图3:
i.在图中标示出b区的Na+和HSO3-的移动方向.
ii.请结合生成H2SO4的电极反应式说明c区除得到浓的硫酸外,还会得到什么物质:SO2.
(1)已知2SO2(g)+O2(g)?2SO3(g)是工业制硫酸的关键反应.如图1为不同温度(T1、T2)下SO2的转化率随时间的变化曲线.

①T1>(填“>”“<”或“=”)T2,判断的依据是温度越高反应速率越快,达到化学平衡的时间越短;该反应为放(填“放”或“吸”)热反应,判断的依据是温度升高时平衡向吸热方向移动,SO2的转化率减小.
②如表为一定温度和压强下,4种投料比[n(SO2):n(O2)]分别为2:18、4:15、7:11和8:10时SO2的平衡转化率.
| 投料比 | a | b | c | d |
| SO2平衡转化率/% | 97.1 | 96.8 | 95.8 | 90.0 |
ii.投料比为8:10时,平衡混合气体中SO3体积分数为50%.
(2)钠碱循环法吸收硫酸厂尾气中的SO2并将其转化为硫酸的工艺如图2:
①吸收池中发生反应的离子方程式是SO2+SO32-+H2O=2HSO3-.
②电解池的构造示意图如图3:
i.在图中标示出b区的Na+和HSO3-的移动方向.
ii.请结合生成H2SO4的电极反应式说明c区除得到浓的硫酸外,还会得到什么物质:SO2.
6.在三个体积相同的密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的是( )
| A. | p (Ne)>p (H2)>p (O2) | B. | p (O2)>p (Ne)>p (H2) | C. | p (H2)>p (O2)>p (Ne) | D. | p (H2)>p (Ne)>p (O2) |
13.KI在经酸化的溶液中被空气氧化生成I2.该反应的速率受温度、酸度、溶剂、试剂浓度等影响,可用淀粉与碘的显色反应来观测该反应的速率.已知,淀粉与碘的显色反应在温度升高时灵敏度会降低,高于75℃则不能显色;淀粉浓度越高显色越灵敏、颜色也越深.
实验小组拟用0.8mol•L-1 KI溶液、0.1mol•L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A-C三组实验,部分实验数据如表:
请回答以下问题:
(1)写出该反应的离子方程式4H++4I-+O2=2I2+2H2O;
(2)为确保A组实验在40℃下进行,实验操作是将量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度.
(3)B组实验中“没出现蓝色”,原因是温度(TB)高于75℃,淀粉与碘不显色.
(4)请你为小组设计D组实验方案,填写空格.以帮助小组完成探究目标.
(5)按你设计的实验数据,请你预测一个t值设计酸体积<10mL时,t预测值要小于同温对比值,设计酸体积>10mL时,t预测值要大于同温对比值,并写出与你预测相对应的探究实验的结论其他条件不变时,酸度越大反应速率越快.
实验小组拟用0.8mol•L-1 KI溶液、0.1mol•L-1H2SO4溶液、淀粉溶液等来探究温度、酸度对上述反应速率的影响,他们做了A-C三组实验,部分实验数据如表:
| 编号 | 温度/℃ | H2SO4体积/mL | KI溶液体积/mL | H2O体积/mL | 淀粉溶液 /mL | 出现蓝色时间/s |
| A | 40 | 10 | 5 | 5 | 1 | 5 |
| B | TB | 10 | 5 | 5 | 1 | 没出现蓝色 |
| C | 5 | 10 | 5 | 5 | 1 | 39 |
| D | t |
(1)写出该反应的离子方程式4H++4I-+O2=2I2+2H2O;
(2)为确保A组实验在40℃下进行,实验操作是将量出的各种溶液分别装在试管中,再将试管全部放在同一水浴中加热,用温度计测量试管中溶液的温度.
(3)B组实验中“没出现蓝色”,原因是温度(TB)高于75℃,淀粉与碘不显色.
(4)请你为小组设计D组实验方案,填写空格.以帮助小组完成探究目标.
(5)按你设计的实验数据,请你预测一个t值设计酸体积<10mL时,t预测值要小于同温对比值,设计酸体积>10mL时,t预测值要大于同温对比值,并写出与你预测相对应的探究实验的结论其他条件不变时,酸度越大反应速率越快.
3.橙花醛是一种香料,其结构简式为(CH3)2C═CHCH2CH2C(CH3)═CHCHO.下列说法正确的是( )
| A. | 橙花醛不能与Br2发生加成反应 | |
| B. | 橙花醛能发生银镜反应 | |
| C. | 1 mol橙花醛最多可以与2 mol H2发生加成反应 | |
| D. | 橙花醛是乙烯的同系物 |
10.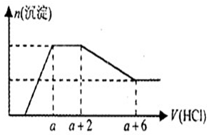 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示.下列判断正确的是( )| A. | 原溶液中一定含有Na2SO4 | |
| B. | 反应后形成的溶液溶质为NaCl | |
| C. | 原溶液中含有CO32-与AlO2-的物质的量比为1:1 | |
| D. | 原溶液中一定含有的离子是OH-,CO32-,SiO32-,AlO2- |
7.有NO、CO2、N2O4三种气体,它们分别都含有0.5mol氧原子,则三种气体的物质的量之比为( )
| A. | 1:2:4 | B. | 1:1:1 | C. | 4:2:1 | D. | 1:2:4 |