题目内容
7.有NO、CO2、N2O4三种气体,它们分别都含有0.5mol氧原子,则三种气体的物质的量之比为( )| A. | 1:2:4 | B. | 1:1:1 | C. | 4:2:1 | D. | 1:2:4 |
分析 结合分子的构成及都含有0.5mol氧原子计算,以此来解答.
解答 解:NO、CO2、N2O4三种气体,它们分别都含有0.5mol氧原子,
即氧原子数相同,
设三种气体的物质的量分别为x、y、,
则x×1=y×2=z×4,
解得x:y:z=4:2:1,
故选C.
点评 本题考查物质的量的计算,把握物质的构成为解答的关键,注意氧原子的物质的量相同即可解答,计算比值不需要计算分子中氧原子的物质的量,简化计算,题目难度不大.

练习册系列答案
相关题目
3.恒温时,在密闭容器中进行可逆反应:N2+3H2?2NH3,达到平衡后,欲使正反应速率增大,可采取的措施是( )
| A. | 缩小容器的容积 | |
| B. | 保持容器的容积不变,通入稀有气体 | |
| C. | 保持容器内压强不变,通入稀有气体 | |
| D. | 及时把生成的NH3分离出去 |
18.某学生设计了如图实验,以下说法错误的是( )


| A. | 该同学的实验目的是分离氯化钠、氯化钙 | |
| B. | 上图括号内的操作步骤均为加热蒸发 | |
| C. | 按此实验方案可得到较纯净的NaCl固体 | |
| D. | 按此实验方案可得到较纯净的CaCl2固体 |
15.下列比较项与依据的化学反应事实对应的是( )
| 比较项 | 依据的化学反应事实 | |
| A | 比较Cl和S的非金属性 | Na2S+2HCl=2NaCl+H2S↑ |
| B | 比较Fe2+和Br-的还原性 | 2FeBr2+3Cl2(过量)=2FeCl3+2Br2 |
| C | 比较氯化银和碘化银溶解度 | AgCl(s)+I-少量(aq)=AgI(s)+Cl-(aq) |
| D | 比较硝酸和硫酸的酸性 | 3Cu+8HNO3(稀)═3Cu(NO3)2+4H2O+2NO↑ Cu和H2SO4(稀)不反应 |
| A. | A | B. | B | C. | C | D. | D |
2.将5mL 10mol/L的硫酸稀释到100mL,所得硫酸溶液的物质的量浓度是( )
| A. | 0.2 mol/L | B. | 0.5 mol/L | C. | 2 mol/L | D. | 5mol/L |
12.在碱性溶液中能大量共存且为无色透明溶液的是( )
| A. | K+ Cl- MnO4- SO42- | B. | Na+ CO32- NO3- SO42- | ||
| C. | Na+ NO3- SO42- HCO3- | D. | Mg2+ SO42- S2- Cl- |
19.关于化学对社会进步和人类文明的贡献,下列说法不正确的是( )
| A. | 化石燃料的直接利用,促进了低碳经济的发展 | |
| B. | 新材料的研制和应用,提高了人们的生活品质 | |
| C. | 合成药物的研发和使用,促进了医疗卫生事业的发展 | |
| D. | 化肥的合理使用提高了农作物产量,缓解了人类粮食危机 |
17.实验室中需要配制2mol/L的NaOH溶液850mL,配制时应选用的容量瓶的规格和称取的NaOH的质量分别是( )
| A. | 950 mL,76 g | B. | 500 mL,80 g | C. | 1000 mL,80 g | D. | 1000 mL,76 g |

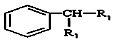 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$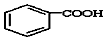
 (-R1、R2表示氢原子或烃基)
(-R1、R2表示氢原子或烃基) ,C的结构简式为CH3CH2OH,
,C的结构简式为CH3CH2OH,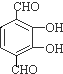 、
、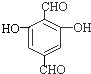 .
. ,反应类型是取代反应.
,反应类型是取代反应.