题目内容
A、B、C是短周期的三种元素,原子序数依次递增,A与C为同族元素,C与A相互间可形成原子个数比为1:2或1:3的化合物,B与A相互间只能形成一种熔点高的化合物,则下列说法正确的是( )
| A、B单质可能是金属,也可能是非金属 |
| B、B与A形成的化合物一定是离子化合物 |
| C、C单质只有氧化性 |
| D、原子半径:C>B>A |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C是短周期的三种元素,原子序数依次递增,A与C为同族元素,C与A相互间可形成原子个数比为1:2或1:3的化合物,则A为氧元素,C为硫元素,B与A相互间只能形成一种熔点高的化合物,则可知该化合物为离子晶体或原子晶体,B可能为钠、镁、铝等金属元素,也可能为硅等非金属元素,据此答题.
解答:
解:A、B、C是短周期的三种元素,原子序数依次递增,A与C为同族元素,C与A相互间可形成原子个数比为1:2或1:3的化合物,则A为氧元素,C为硫元素,B与A相互间只能形成一种熔点高的化合物,则可知该化合物为离子晶体或原子晶体,B可能为钠、镁、铝等金属元素,也可能为硅等非金属元素,
A、由上面的分析可知,B单质可能是金属,也可能是非金属,故A正确;
B、由于B可能是金属元素,也可能为非金属元素,所以与A形成的化合物可能是离子晶体,也可能为原子晶体,故B错误;
C、硫既有一定的氧化性,又有一定的还原性,故C错误;
D、由于B元素在第三周期,原子序数小于硫,所以半径大于硫原子,故D错误;
故选A.
A、由上面的分析可知,B单质可能是金属,也可能是非金属,故A正确;
B、由于B可能是金属元素,也可能为非金属元素,所以与A形成的化合物可能是离子晶体,也可能为原子晶体,故B错误;
C、硫既有一定的氧化性,又有一定的还原性,故C错误;
D、由于B元素在第三周期,原子序数小于硫,所以半径大于硫原子,故D错误;
故选A.
点评:本题主要考查了元素周期律、元素周期表、晶体的性质,中等难度,解题的关键是元素的推断,答题时注意B元素不确定,只是在一定的范围内,要考滤B可能的元素及性质.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
在合成氨工业中,为增加氨气的日产量,在过程中与平衡移动无关的是( )
| A、不断分离出液氨 |
| B、使用催化剂 |
| C、采用500℃的高温 |
| D、采用20-50Mp的压强 |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、1molNa变成Na+时失去的电子数为NA |
| B、12g12C中所含12C的数目为NA |
| C、CaCl2溶液中若含有1.5NA个Ca2+,则含有3NA个Cl- |
| D、11.2LN2中含有的氮原子数目为NA |
某同学在实验室进行了如图所示的实验,下列说法中错误的是( )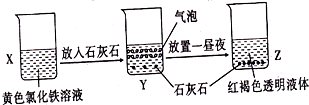

| A、利用过滤的方法,可将Z中固体与液体分离 |
| B、X、Z烧杯中分散质相同 |
| C、Y中反应的离子方程式为3CaCO3+2Fe3++3H2O=2Fe(OH)3+3 CO2↑+3 Ca2+ |
| D、Z中分散系能产生丁达尔效应 |
黄铜矿(CuFeS2)常用于提炼金属铜.黄铜矿焙烧过程中所发生的反应比较复杂,其中主要反应之一的化学方程式为2CuFeS2+O2═□+2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )
| A、方框中的物质应为Cu2S |
| B、该反应的部分产物可用于硫酸工业 |
| C、反应中SO2既是氧化产物又是还原产物 |
| D、反应中若有1 mol SO2生成,则一定有4 mol电子发生转移 |