题目内容
下列说法正确的是( )
| A、气体摩尔体积的值为22.4L/mol |
| B、阿伏伽德罗常数的值为6.02×1023 |
| C、1mol硫酸的质量为98g,硫酸的摩尔质量为98g/mol |
| D、将40 g NaOH溶解于1 L水中所得溶液中溶质的物质的量浓度为1 mol?L-1 |
考点:气体摩尔体积,摩尔质量
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据气体摩尔体积与标况下的气体摩尔体积的关系判断;
B、6.02×1023是阿伏伽德罗常数的近似值;
C、根据m=n=×M,摩尔质量在数值上等于其相对分子质量或相对原子质量;
D、溶液体积不等于溶剂体积.
B、6.02×1023是阿伏伽德罗常数的近似值;
C、根据m=n=×M,摩尔质量在数值上等于其相对分子质量或相对原子质量;
D、溶液体积不等于溶剂体积.
解答:
解:A、单位物质的量的气体所占有的体积为气体摩尔体积,标准状况下气体的摩尔体积约为22.4L/mol,故A错误;
B、阿伏伽德罗常数的近似值为6.02×1023,故B错误;
C、硫酸的摩尔质量为98g/mol,1mol硫酸的质量为98g,故C正确;
D、将40 g NaOH溶解于1 L水中,所得溶液的体积不等于1 L,溶质的物质的量浓度不为1 mol?L-1,故D错误;
故选C.
B、阿伏伽德罗常数的近似值为6.02×1023,故B错误;
C、硫酸的摩尔质量为98g/mol,1mol硫酸的质量为98g,故C正确;
D、将40 g NaOH溶解于1 L水中,所得溶液的体积不等于1 L,溶质的物质的量浓度不为1 mol?L-1,故D错误;
故选C.
点评:本题考查物质的量的有关概念,题目难度中等,要准确解答好这类题目,要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
相关题目
 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A、a点对应的沉淀只有BaSO4 |
| B、c点溶液铝元素以AlO2- 的形式存在 |
| C、b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ |
| D、c点加入Ba(OH)2溶液的体积为200 mL |
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,分别与物质的量浓度相同,体积相同的三份AgNO3溶液恰好反应,用去的三种溶液的体积比为( )
| A、1:2:3 |
| B、6:3:2 |
| C、3:2:1 |
| D、1:1:1 |
设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A、氧气和臭氧的混合物1.6g中含有6.02×1022个氧原子 |
| B、2.8克氮气和一氧化碳混合气体的原子数目为0.2NA |
| C、1.12L氯气中含有6.02×1022个氯原子 |
| D、标准状况下,1.12L的H2O所含的原子数大于0.15NA |
用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2 NA |
| C、常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2 NA |
| D、常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6 NA |
下列热化学方程式中△H代表燃烧热的是( )
A、CH4 ( g )+
| ||
B、S ( s )+
| ||
| C、C6H12O6 ( s )+6O2 ( g )=6CO2 (g)+6H2O ( l )△H3 | ||
| D、2CO ( g )+O2( g )=2CO2 ( g )△H4 |
若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为( )
| A、CH4?14H2O | ||
| B、CH4?8H2O | ||
C、CH4?7
| ||
| D、CH4?6H2O |
下列粒子不能直接构成物质的是( )
| A、原子 | B、分子 | C、离子 | D、电子 |

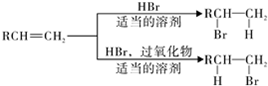
 )的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任用).合成路线流程图示例如下: