题目内容
若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为( )
| A、CH4?14H2O | ||
| B、CH4?8H2O | ||
C、CH4?7
| ||
| D、CH4?6H2O |
考点:不同晶体的结构微粒及微粒间作用力的区别,复杂化学式的确定
专题:计算题
分析:根据题意,在“可燃冰”晶体中,每8个笼由46个H2O分子构成框架,其中容纳6个CH4分子和2个H2O分子.可判断每8个笼共48个H2O分子和6个CH4分子;据此推断可表示可燃冰的平均组成的化学式.
解答:
解:“可燃冰”是一种晶体,晶体中平均每46个H2O分子构建8个笼,每个笼内可容纳一个CH4分子,另外2个笼被游离的H2O分子填充,因此6个笼中有6个甲烷分子,水分子46+2=48,共48个H2O,则“可燃冰”平均分子组成可表示为:6CH4?48H2O,即CH4?8H2O;
故选B.
故选B.
点评:本题是一道应用型信息题,解题时要把握题给信息的实质,结合新旧知识,对需解答的问题进行分析、辨别,它侧重考查学生接受并运用新信息解决问题的能力,题目难度中等.

练习册系列答案
相关题目
下列变化中,属于氧化还原反应又能通过一步反应实现的是( )
| A、Na→Na2O2 |
| B、Si→H2SiO3 |
| C、CuSO4→CuCl2 |
| D、Cu(OH)2→CuO |
下列化学用语中,书写正确的是( )
| A、乙烯的结构简式:CH2CH2 |
| B、氮气的结构式:N≡N |
C、水分子的电子式: |
D、硫原子的结构示意图: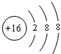 |
下列说法正确的是( )
| A、气体摩尔体积的值为22.4L/mol |
| B、阿伏伽德罗常数的值为6.02×1023 |
| C、1mol硫酸的质量为98g,硫酸的摩尔质量为98g/mol |
| D、将40 g NaOH溶解于1 L水中所得溶液中溶质的物质的量浓度为1 mol?L-1 |
下列说法正确的是( )
| A、测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度 |
| B、在101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,H2的燃烧热为:-285.8kJ?mol-1 |
| C、在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ?mol-1 |
| D、生成物总能量一定低于反应物总能量,同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
由钾和氧组成的某种离子晶体中,阳离子与阴离子的质量之比为13:8,其中阴离子只有过氧离子(O22-)和超氧离子(O2-)两种,则过氧离子与超氧离子的物质的量之比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、1:3 |
下列化学式可称为分子式的是( )
| A、NaNO3 |
| B、NH4Cl |
| C、H2SO4 |
| D、SiO2 |
 在过量的盐酸中加入等质量的锌在不同的试验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的试验( )
在过量的盐酸中加入等质量的锌在不同的试验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的试验( ) | 组别 | c(HCl)(mol?L-1) | 温度(℃) | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 粉末状 |
| 4 | 2.5 | 30 | 粉末状 |
| A、4-3-1-2 |
| B、1-2-3-4 |
| C、1-2-4-3 |
| D、3-4-2-1 |
