题目内容
4.从环己烷可制备1,4-环己二醇,下列有关7步反应(其中无机产物都已略去),其中有2步属于取代反应,2步属于消去反应,3步属于加成反应.试回答:
(1)化合物的结构简式:B
 ,C
,C
(2)反应⑥所用试剂和条件是氢氧化钠的水溶液、加热
(3)反应⑤的方程式是
 .
.
分析 环己烷和氯气发生取代反应生成 ,
, 在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为:
在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为: ,A和氯气反应生成B,B发生消去反应生成
,A和氯气反应生成B,B发生消去反应生成 ,所以B的结构简式为
,所以B的结构简式为 ,则A和氯气发生加成反应生成B,
,则A和氯气发生加成反应生成B, 和溴发生1,4-加成反应生成
和溴发生1,4-加成反应生成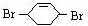 ,
,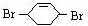 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为 ,
, 和氢气发生加成反应生成
和氢气发生加成反应生成 ,据此答题.
,据此答题.
解答 解:环己烷和氯气发生取代反应生成 ,
, 在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为:
在氢氧化钠的醇溶液、加热条件下发生消去反应生成A,则A的结构简式为: ,A和氯气反应生成B,B发生消去反应生成
,A和氯气反应生成B,B发生消去反应生成 ,所以B的结构简式为
,所以B的结构简式为 ,则A和氯气发生加成反应生成B,
,则A和氯气发生加成反应生成B, 和溴发生1,4-加成反应生成
和溴发生1,4-加成反应生成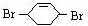 ,
,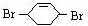 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为 ,
, 和氢气发生加成反应生成
和氢气发生加成反应生成 ,
,
(1)根据上面的分析可知,B的结构简式为 ,C为
,C为 ,
,
故答案为: ;
; ;
;
(2)反应⑥为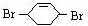 在氢氧化钠的水溶液、加热条件下发生取代反应生成C为
在氢氧化钠的水溶液、加热条件下发生取代反应生成C为 ,所用试剂和条件是,
,所用试剂和条件是,
故答案为:氢氧化钠的水溶液、加热;
(3)反应⑤为 和溴水发生1,4加成生成
和溴水发生1,4加成生成 ,反应方程式为
,反应方程式为 ,
,
故答案为: .
.
点评 本题考查有机物推断,涉及环烷烃、氯代烃、环烯烃、醇之间的转化,明确物质的官能团及其性质是解本题关键,采用正逆结合的方法进行推断,注意反应条件,反应条件不同会导致其产物不同.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
12.用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,48g O2和O3混合气体中含有原子数3NA | |
| B. | 2 mol SO2 和1 mol O2在一定条件下反应能生成2mol SO3 | |
| C. | 17g羟基(-OH)所含电子数为10NA | |
| D. | 0.1mol/L稀硫酸中含有SO42-离子个数为0.1NA |
19.与100mL 0.5mol•L-1NaCl溶液中的Cl-的物质的量浓度相同的是( )
| A. | 100mL 0.5 mol•L-1MgCl2溶液 | B. | 100mL 0.5mol•L-1KClO3溶液 | ||
| C. | 200mL 0.25 mo l•L-1 KCl溶液 | D. | 200mL 0.5mol•L-1 HCl溶液 |
9.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,Na2O2与足量的水反应,共生成0.2mol O2,转移的电子数目为0.8NA | |
| B. | 16g16O2和18 g18O2中含有的质子数均为8NA | |
| C. | 1 mol Fe与足量的稀硝酸反应,转移电子数为2NA | |
| D. | 标准状况下,2.24 L Cl2溶于水所得溶液中含有的氯离子数为0.1NA |
16.一定量的Fe与过量的稀硫酸反应,为了减缓反应速率又不影响生成氢气的总量,不可以采取的措施是( )
| A. | 加入K2SO4溶液 | B. | 加入CH3COONa固体 | ||
| C. | 加一定量水 | D. | 加入KNO3溶液 |
13.日常生活和工业生产中常用到漂白剂,下列物质的溶液具有漂白作用的是( )
| A. | CuSO4 | B. | CaCl2 | C. | Na2SO4 | D. | Ca(ClO)2 |
14.下列物质能通过化合反应直接制得的是( )
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl ⑤Fe(OH)3.
①FeCl2 ②H2SO4 ③NH4NO3 ④HCl ⑤Fe(OH)3.
| A. | 只有①②③ | B. | 只有②③ | C. | 只有①③④ | D. | 全部 |
