题目内容
9.下列反应的离子方程式书写正确的是( )| A. | 氯气和水的反应:C12+H2O═2H++Clˉ+ClOˉ | |
| B. | 向Al2(SO4)2溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 硫酸氢铵溶液中加入过量氢氧化钡溶液:Ba2++SO42-═BaSO4↓ | |
| D. | 铜片加入稀硝酸中:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
分析 A.次氯酸为弱酸,离子方程式中次氯酸不能拆开;
B.氨水为弱碱,二者反应生成氢氧化铝沉淀和硫酸铵;
C.氢氧化钡过量,氢离子、铵根离子都参与反应;
D.铜与稀硝酸反应生成的是NO气体.
解答 解:A.氯气与水反应生成氯化氢和次氯酸,次氯酸小于保留分子式,正确的离子方程式为C12+H2O═H++Cl-+HClO,故A错误;
B.向Al2(SO4)2溶液中加入过量的氨水,反应的离子方程式为:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B正确;
C.向硫酸氢铵溶液中加入过量氢氧化钡溶液,铵根离子、氢离子和硫酸根离子都参与反应,正确的离子反应为NH4++2OH-+H++Ba2++SO42-═BaSO4↓+NH3•H2O+H2O,故C错误;
D.铜与稀硝酸反应生成硝酸铜、一氧化氮气体和水,正确的离子方程式为:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
19.短周期元素W、X、Y、Z的原子序数依次增大,其中W的原子核中只有6个质子;X可与W形成两种常见的气体WX和WX2;Y是短周期元素中原子半径最大的元素;Z与Y形成的化合物的水溶液呈中性.下列叙述正确的是( )
| A. | Y位于第三周期,ⅦA族 | B. | 单质沸点:W>Y | ||
| C. | 气体氢化物稳定性:W>Z | D. | 离子半径:X<Y |
20.化学与生活密切相关,下列生活中的常见物质按酸碱性的一定顺序依次排列正确的是( )
| A. | 厕所清洁剂、醋、肥皂、厨房清洁剂 | B. | 厕所清洁剂、厨房清洁剂、醋、肥皂 | ||
| C. | 醋、厕所清洁剂、肥皂、厨房清洁剂 | D. | 厨房清洁剂、醋、肥皂、厕所清洁剂 |
17.关于Na2CO3和NaHCO3的比较中不正确的是( )
| A. | NaHCO3比Na2CO3热稳定性差 | |
| B. | NaHCO3比Na2CO3与稀盐酸反应的速度快 | |
| C. | 在相同温度下,Na2CO3的溶解度大于NaHCO3 | |
| D. | Na2CO3能使澄清石灰水变浑浊,而NaHCO3不行 |
4.下列各组离子能大量共存的是( )
| A. | H+、Na+、HCO${\;}_{3}^{-}$、Cl- | B. | Mg2+、NO${\;}_{3}^{-}$、Na+、OH- | ||
| C. | Ca2+、Cl-、CO${\;}_{3}^{2-}$、OH- | D. | Na+、Cl-、K+、NO${\;}_{3}^{-}$ |
2.下列有机物的命名中,正确的是( )
| A. | 3,3二甲基4乙基戊烷 | B. | 2,5,5三甲基己烷 | ||
| C. | 2,3二甲基丁烯 | D. | 3甲基1戊炔 |
9.T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B、C物质的量变化如下图(Ⅰ)所示.若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如下图(Ⅱ)所示.下列叙述正确的是( )
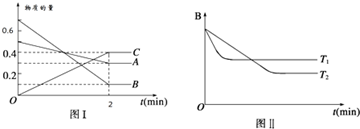

| A. | 2min内A的化学反应速率为0.1 mol/(L•min) | |
| B. | 在反应达平衡时,保持其他条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动 | |
| C. | 在反应达平衡时,其他条件不变,升高温度,正逆反应速率都增大,且A的转化率增大 | |
| D. | 图(I)中,达平衡时,A的体积分数为37.5% |
7.下列物质的鉴别方法正确的有( )
| A. | 用硝酸银溶液区分碳酸钠和氯化钠 | |
| B. | 用硝酸钡溶液区分碳酸钠和硫酸钠 | |
| C. | 用氯化钙溶液区分碳酸钠和碳酸氢钠 | |
| D. | 用盐酸区分氢氧化钠和氯化钠 |