题目内容
部分短周期元素的原子半径及常见化合价如表:
根据要求回答问题(如需填化学用语的,请用各元素的元素符号表示)
(1)X元素在元素周期表的位置是 .
(2)R的气态氢化物比X的气态氢化物 (填稳定或不稳定).
(3)写出M的单质与ZT2反应的化学方程式 .
(4)Q的最高价氧化物在现代通信的重要用途是 .
(5)己知XO2在500℃,1大气压下被氧气氧化,每生成1mol气态XO3,放出98.3kJ热量,该反应的热化学方程式是
(6)工业上用Z的单质与水蒸汽反应制水煤气,则该反应的平衡常数表达式K= .
| 元素代号 | Z | M | Q | R | T | X |
| 原子半径/nm | 0.077 | 0.130 | 0.111 | 0.099 | 0.073 | 0.102 |
| 常见化合价 | +4,-4 | +2 | +4,-4 | -1,+7 | -2 | +6,-2 |
(1)X元素在元素周期表的位置是
(2)R的气态氢化物比X的气态氢化物
(3)写出M的单质与ZT2反应的化学方程式
(4)Q的最高价氧化物在现代通信的重要用途是
(5)己知XO2在500℃,1大气压下被氧气氧化,每生成1mol气态XO3,放出98.3kJ热量,该反应的热化学方程式是
(6)工业上用Z的单质与水蒸汽反应制水煤气,则该反应的平衡常数表达式K=
考点:元素周期律和元素周期表的综合应用
专题:
分析:主族元素中,元素最高化合价与其族序数相等,最低负价=族序数-8,同一周期元素,原子半径随着原子序数增大而减小,同一主族元素,原子半径随着原子序数增大而增大,根据元素化合价知,Z、Q属于第IVA族,且Z原子半径小于Q,所以Z是C元素、Q是Si元素;
M是第IIA族元素,M原子半径大于Q,所以M是Mg元素;
R为第VIIA族,因为R有正化合价,所以R是Cl元素;
T和X属于第VIA族元素,T原子半径小于X,所以T是O元素、X是S元素,
再结合物质结构、性质分析解答.
M是第IIA族元素,M原子半径大于Q,所以M是Mg元素;
R为第VIIA族,因为R有正化合价,所以R是Cl元素;
T和X属于第VIA族元素,T原子半径小于X,所以T是O元素、X是S元素,
再结合物质结构、性质分析解答.
解答:
解:主族元素中,元素最高化合价与其族序数相等,最低负价=族序数-8,同一周期元素,原子半径随着原子序数增大而减小,同一主族元素,原子半径随着原子序数增大而增大,根据元素化合价知,Z、Q属于第IVA族,且Z原子半径小于Q,所以Z是C元素、Q是Si元素;
M是第IIA族元素,M原子半径大于Q,所以M是Mg元素;
R为第VIIA族,因为R有正化合价,所以R是Cl元素;
T和X属于第VIA族元素,T原子半径小于X,所以T是O元素、X是S元素,
(1)X是S元素,X元素在元素周期表的位置是第三周期第VIA族,故答案为:第三周期第VIA族;
(2)非金属性R>S,所以R的气态氢化物比X的气态氢化物稳定,故答案为:稳定;
(3)M是Mg元素,Z是C元素、T是O元素,ZT2是CO2,镁在二氧化碳中燃烧生成C和MgO,所以M的单质与ZT2反应的化学方程式2Mg+CO2
2MgO+C,故答案为:2Mg+CO2
2MgO+C;
4)Q是Si元素,Q的最高价氧化物在现代通信的重要用途是作光导纤维,是利用光的全反射原理,故答案为:光导纤维;
(5)X是S元素,SO2在500℃,1大气压下被氧气氧化,每生成1mol气态SO3,放出98.3kJ热量,则生成2mol三氧化硫放出196.6kJ热量,该反应的热化学方程式是2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,故答案为:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1;
(6)Z为C元素,工业上用Z的单质与水蒸汽反应制水煤气,反应方程式为C(s)+H2O(g)?CO(g)+H2(g),则该反应的平衡常数表达式K=
,
故答案为:
.
M是第IIA族元素,M原子半径大于Q,所以M是Mg元素;
R为第VIIA族,因为R有正化合价,所以R是Cl元素;
T和X属于第VIA族元素,T原子半径小于X,所以T是O元素、X是S元素,
(1)X是S元素,X元素在元素周期表的位置是第三周期第VIA族,故答案为:第三周期第VIA族;
(2)非金属性R>S,所以R的气态氢化物比X的气态氢化物稳定,故答案为:稳定;
(3)M是Mg元素,Z是C元素、T是O元素,ZT2是CO2,镁在二氧化碳中燃烧生成C和MgO,所以M的单质与ZT2反应的化学方程式2Mg+CO2
| ||
| ||
4)Q是Si元素,Q的最高价氧化物在现代通信的重要用途是作光导纤维,是利用光的全反射原理,故答案为:光导纤维;
(5)X是S元素,SO2在500℃,1大气压下被氧气氧化,每生成1mol气态SO3,放出98.3kJ热量,则生成2mol三氧化硫放出196.6kJ热量,该反应的热化学方程式是2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,故答案为:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1;
(6)Z为C元素,工业上用Z的单质与水蒸汽反应制水煤气,反应方程式为C(s)+H2O(g)?CO(g)+H2(g),则该反应的平衡常数表达式K=
| C(H2).C(CO) |
| C(H2O) |
故答案为:
| C(H2).C(CO) |
| C(H2O) |
点评:本题侧重考查原子结构、元素周期表结构、元素周期律等知识点,正确推断元素是解本题关键,知道元素化合价与元素族序数的关系,熟练掌握元素化合物知识,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
人们在日常生活中大量使用各种高分子材料,下列说法正确的是( )
| A、天然橡胶易溶于水 |
| B、羊毛是合成高分子材料 |
| C、聚乙烯塑料是天然高分子材料 |
| D、酚醛塑料(俗称电木)不可以进行热修补 |
某溶液中可能含有SO42-、CO32-、Cl-.为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是( )
| A、稀硫酸 |
| B、稀盐酸 |
| C、NaOH溶液 |
| D、NaNO3溶液 |
如图是在待镀铁制品上镀铜的实验装置,则下列说法正确的是( )
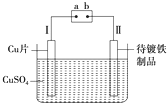

| A、Ⅰ极上铜放电而逐渐消耗 |
| B、电源a极为负极 |
| C、Ⅱ极上发生的电极反应为Fe-2e-═Fe2+ |
| D、Ⅱ极上Cu2+放电而使溶液中Cu2+浓度逐渐变小 |
下列反应中一定释放热量的是( )
| A、置换反应 | B、化合反应 |
| C、分解反应 | D、中和反应 |
下列反应的离子方程式书写正确的是( )
| A、氧化铜与盐酸反应 O2-+2H+=H2O |
| B、二氧化碳通入足量氢氧化钠溶液中:CO2+OH-=HCO3- |
| C、铝片与硫酸铜溶液反应:2Al+3Cu2+=2Al3++3Cu |
| D、氢氧化钡溶液与稀H2SO4 反应:H++OH-+Ba2++SO42-=BaSO4↓+H2O |
 ,请回答下列问题.
,请回答下列问题. 如图为某市售氨水试剂标签上的部分数据.试计算:
如图为某市售氨水试剂标签上的部分数据.试计算: