题目内容
下列反应的离子方程式书写正确的是( )
| A、氧化铜与盐酸反应 O2-+2H+=H2O |
| B、二氧化碳通入足量氢氧化钠溶液中:CO2+OH-=HCO3- |
| C、铝片与硫酸铜溶液反应:2Al+3Cu2+=2Al3++3Cu |
| D、氢氧化钡溶液与稀H2SO4 反应:H++OH-+Ba2++SO42-=BaSO4↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氧化铜为氧化物,离子方程式中不能拆开,需要保留化学式;
B.氢氧化钠溶液足量,反应生成碳酸根离子和水,不是生成碳酸氢根离子;
C.铝与硫酸铜溶液反应生成硫酸铝和铜,根据电荷守恒、质量守恒判断;
D.氢氧根离子、氢离子与硫酸、氢氧化钡的化学式组成不相符.
B.氢氧化钠溶液足量,反应生成碳酸根离子和水,不是生成碳酸氢根离子;
C.铝与硫酸铜溶液反应生成硫酸铝和铜,根据电荷守恒、质量守恒判断;
D.氢氧根离子、氢离子与硫酸、氢氧化钡的化学式组成不相符.
解答:
解:A.氧化铜与盐酸反应反应生成生成氯化铁和水,反应的离子方程式为:CuO+2H+=H2O+Cu2+,故A错误;
B.二氧化碳通入足量氢氧化钠溶液中,反应生成碳酸根离子和水,反应的离子方程式为:CO2+2OH-=H2O+CO32-,故B错误;
C.铝片与硫酸铜溶液反应生成硫酸铝和铜单质,反应的离子方程式为:2Al+3Cu2+=2Al3++3Cu,故C正确;
D.氢氧化钡溶液与稀H2SO4反应生成硫酸钡和水,正确的离子方程式为:2H++2OH-+Ba2++SO42-=BaSO4↓+2H2O,故D错误;
故选C.
B.二氧化碳通入足量氢氧化钠溶液中,反应生成碳酸根离子和水,反应的离子方程式为:CO2+2OH-=H2O+CO32-,故B错误;
C.铝片与硫酸铜溶液反应生成硫酸铝和铜单质,反应的离子方程式为:2Al+3Cu2+=2Al3++3Cu,故C正确;
D.氢氧化钡溶液与稀H2SO4反应生成硫酸钡和水,正确的离子方程式为:2H++2OH-+Ba2++SO42-=BaSO4↓+2H2O,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
下列物质中,所含分子的物质的量最多的是( )
| A、0.05 mol CCl4 |
| B、4℃[ρ(H2O)=1g?mL-1]时,3.6 mL H2O |
| C、6.02×1022个HCl分子 |
| D、标准状况下,58.5 g的NaCl晶体 |
下列叙述中,正确的是( )
| A、1 mol 乙烯分子中含有共价键的数目为7NA |
| B、1 mol甲基(-CH3)中含有电子的数目为10NA |
| C、标准状况下,1L戊烷在空气中完全燃烧生成5/22.4 L的CO2 |
| D、14 g乙烯和丙烯的混合物中含有碳原子的数目为NA |
下列离子方程式正确的是( )
| A、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
| B、氧化铝溶解在NaOH溶液中:3H2O+Al2O3+2OH-?=2[Al(OH)4]-? |
| C、硫酸铝溶液与氢氧化钡溶液反应,使SO42-恰好沉淀完全Al3++SO42-?+Ba2++3OH-=BaSO4↓+Al(OH)3↓ |
| D、在漂白粉配制成的溶液中通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
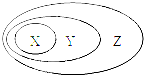 用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )