题目内容
如图是在待镀铁制品上镀铜的实验装置,则下列说法正确的是( )
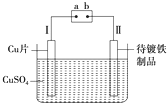

| A、Ⅰ极上铜放电而逐渐消耗 |
| B、电源a极为负极 |
| C、Ⅱ极上发生的电极反应为Fe-2e-═Fe2+ |
| D、Ⅱ极上Cu2+放电而使溶液中Cu2+浓度逐渐变小 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在铁上镀铜,铁作阴极,铜作阳极,
A.阳极上金属铜失电子发生氧化反应;
B.连接阴极的电源电极是负极;
C.铁电极上铜离子得电子发生还原反应;
D.根据阴阳极上得失电子的微粒来确定溶液中铜离子浓度是否变化.
A.阳极上金属铜失电子发生氧化反应;
B.连接阴极的电源电极是负极;
C.铁电极上铜离子得电子发生还原反应;
D.根据阴阳极上得失电子的微粒来确定溶液中铜离子浓度是否变化.
解答:
解:在铁上镀铜,铁作阴极,铜作阳极,
A.阳极上金属铜失电子生成铜离子而发生氧化反应进入溶液,则阳极材料逐渐消耗,故A正确;
B.连接阴极的电源电极是负极,所以b是负极,故B错误;
C.铁电极上铜离子得电子发生还原反应生成铜单质,电极反应式为Cu2++2e-=Cu,故C错误;
D.阴极上铜离子得电子生成铜单质,阳极上铜失电子生成铜离子进入溶液,阴阳极上得失电子相等,所以阳极消耗的铜等于阴极上析出的铜,则电解质溶液中铜离子浓度不变,故D错误;
故选A.
A.阳极上金属铜失电子生成铜离子而发生氧化反应进入溶液,则阳极材料逐渐消耗,故A正确;
B.连接阴极的电源电极是负极,所以b是负极,故B错误;
C.铁电极上铜离子得电子发生还原反应生成铜单质,电极反应式为Cu2++2e-=Cu,故C错误;
D.阴极上铜离子得电子生成铜单质,阳极上铜失电子生成铜离子进入溶液,阴阳极上得失电子相等,所以阳极消耗的铜等于阴极上析出的铜,则电解质溶液中铜离子浓度不变,故D错误;
故选A.
点评:本题考查了电解池原理,根据阴阳极上得失电子、阴阳极与原电池正负极的关系来分析解答,注意电镀和电解精炼不同,电镀上电解质溶液中金属阳离子浓度不变,电解精炼时电解质溶液中与阴极相同元素的金属阳离子浓度减小,为易错点.

练习册系列答案
相关题目
将HBr(g)充入恒容密闭容器,恒温下发生反应2HBr(g)?H2(g)+Br2(g)△H>0,平衡时HBr(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时HBr(g)的转化率为b.下列a与b关系正确的是( )
| A、a>b | B、a=b |
| C、a<b | D、无法确定 |
主族元素M、R形成的简单离子M2-离子与R+离子的核外电子数之和为20,下列说法正确的是( )
| A、M与R的原子序数之差可能等于7 |
| B、若M在第3周期,则R一定在第2周期 |
| C、M2-的离子半径可能比R+的离子半径小 |
| D、两种离子结合形成的化合物可能是共价化合物 |
下列比较正确的是( )
| A、第一电离能:I1(P)>I1(S) |
| B、离子半径:r(Al3+)>r(O2-) |
| C、能量:E(4s)>E(3d) |
| D、电负性:K元素>Na元素 |
下列各组物质中,前者为强电解质,后者为弱电解质的是( )
| A、氯化钠,浓氨水 |
| B、氢氧化钠,水 |
| C、硫酸,硫酸钡 |
| D、氯化银,二氧化硫 |
关于化学反应的△H的理解正确的是( )
| A、△H>0的反应是吸热反应 |
| B、△H=ΣH(反应物)-ΣH(生成物) |
| C、所有化学反应的△H都可以通过实验测出 |
| D、△H=反应中化学键形成时吸收的总能量-反应中化学键断裂时放出的总能量 |
某气体的质量为3.2g,含有的是3.01×1022个分子,则该气体的相对分子质量是( )
| A、32 |
| B、64 |
| C、32 g/mol |
| D、64 g/mol |
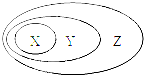 用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用图表示的一些物质或概念之间的从属或包含关系中,错误的是( )