题目内容
5.在pH=0的无色溶液中能大量共存的离子组是( )| A. | Na+、Ca2+、Cl-、AlO2- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | NH4+.、Mg2+、SO42-、Cl- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,pH=0的溶液中存在大量氢离子,
A.偏铝酸根离子与氢离子反应;
B.氢氧根离子与氢离子反应生成水;
C.铜离子为有色离子;
D.四种离子之间不反应,都不与氢离子反应,且为无色溶液.
解答 解:无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,pH=0的溶液为酸性溶液,溶液中存在大量氢离子,
A.AlO2-与酸性溶液中的氢离子反应,在溶液中不能大量共存,故A错误;
B.OH-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Cu2+为有色离子,在溶液中不能大量共存,故C错误;
D.NH4+、Mg2+、SO42-、Cl-之间不发生反应,都是无色离子,都不与氢离子反应,在溶液中可以大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
15.如图所示的实验,发现烧杯中酸性KMn04溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeS04溶液,溶液呈血红色.判断下列说法中不正确的是( )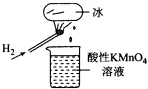

| A. | 该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 | |
| B. | 该条件下H2燃烧的产物中可能含有一定量的H2O2、HO2等 | |
| C. | 将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性 | |
| D. | 酸性FeSO4溶液中加入双氧水的离子反应为:2Fe 2++H2O2+2H+=2Fe3++2H20 |
16. 目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应.某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验.
目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应.某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验.
[实验I]确定硫的质量:
按图连接装置,检查好装置的气密性后,在硬质玻璃管A中放入1.0g铁硫簇结构(含有部分不反应的杂质),在试管B中加入50mL 0.100mol•L-1的酸性KMn04溶液,在试管C中加入品红溶液.通入空气并加热,发现固体逐渐转变为红棕色.待固体完全转化后,将B中溶液转移至250mL容量瓶,洗涤试管B后定容.取25.00mL该溶液用0.01mol•L-1的草酸(H2C204)溶液滴定剩余的KMn04.记录数据如下:
相关反应:①2MnO4-+2H20+5S02═2Mn2++5S042-+4H+
②2MnO4-+6H++5H2C2O4═2Mn2++l0CO2↑+8H20
[实验Ⅱ]确定铁的质量:
将实验I硬质玻璃管A中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经充分灼烧得0.6g固体.
试回答下列问题:
(1)实验I中判断滴定终点的方法是加入最后一滴草酸,溶液紫色褪去,且半分钟不变色.
(2)实验I中,试管C中品红溶液的作用是检验二氧化硫是否被酸性高锰酸钾完全吸收.
有同学提出,撤去C装置对实验没有影响,你的看法是同意(选填“同意”或“不同意”),理由是若B中高锰酸钾溶液的紫色不褪去,说明二氧化硫被吸收完全.
(3)根据实验I和实验Ⅱ中的数据可确定该铁硫簇结构的化学式为Fe3S4.
[问题探究]滴定过程中,细心的小明发现该KMnO4溶液颜色褪去的速率较平常滴定时要快
得多.为研究速率加快的原因,小明继续进行了下列实验,实验数据如下表:
(4)分析上述数据知,滴定过程中反应速率较平常滴定时要快的一种可能原因是生成锰离子对反应起催化作用(或反应放热使温度升高,加快反应速率).
 目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应.某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验.
目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境,这种环境系统中普遍存在铁硫簇结构,如Fe2S2、Fe4S4、Fe8S7等,这些铁硫簇结构参与了生命起源的相关反应.某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验.[实验I]确定硫的质量:
按图连接装置,检查好装置的气密性后,在硬质玻璃管A中放入1.0g铁硫簇结构(含有部分不反应的杂质),在试管B中加入50mL 0.100mol•L-1的酸性KMn04溶液,在试管C中加入品红溶液.通入空气并加热,发现固体逐渐转变为红棕色.待固体完全转化后,将B中溶液转移至250mL容量瓶,洗涤试管B后定容.取25.00mL该溶液用0.01mol•L-1的草酸(H2C204)溶液滴定剩余的KMn04.记录数据如下:
| 滴定次数 | 待测溶液体积/mL | 草酸溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.50 | 23.70 |
| 2 | 25.00 | 1.02 | 26.03 |
| 3 | 25.00 | 0.00 | 24.99 |
②2MnO4-+6H++5H2C2O4═2Mn2++l0CO2↑+8H20
[实验Ⅱ]确定铁的质量:
将实验I硬质玻璃管A中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经充分灼烧得0.6g固体.
试回答下列问题:
(1)实验I中判断滴定终点的方法是加入最后一滴草酸,溶液紫色褪去,且半分钟不变色.
(2)实验I中,试管C中品红溶液的作用是检验二氧化硫是否被酸性高锰酸钾完全吸收.
有同学提出,撤去C装置对实验没有影响,你的看法是同意(选填“同意”或“不同意”),理由是若B中高锰酸钾溶液的紫色不褪去,说明二氧化硫被吸收完全.
(3)根据实验I和实验Ⅱ中的数据可确定该铁硫簇结构的化学式为Fe3S4.
[问题探究]滴定过程中,细心的小明发现该KMnO4溶液颜色褪去的速率较平常滴定时要快
得多.为研究速率加快的原因,小明继续进行了下列实验,实验数据如下表:
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | 5.0(另加少量可溶于水的MnSO4粉末) | 2.0 | 4 |
| 3 | 60 | 5.0 | 2.0 | 25 |
20.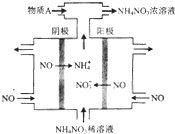 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.
(1)电解NO制备NH4NO3,其工作原理如图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是NH3,理由是:根据反应:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3.
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3?)、c(NO2?)和c(CH3COO?)由大到小的顺序为c(NO3-)>c(NO2-)>c(CH3COO-)(已知HNO2的电离常数Ka=7.1×10-4mol/L,CH3COOH的电离常数Ka=1.7×10-5mol/L).可使溶液A和溶液B的pH相等的方法是bc.
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)100℃时,将0.400mol 的NO2气体充入2L抽空的密闭容器中,发生反应2NO2(g)?N2O4(g)△H<0.每隔一定时间就对该容器内的物质进行分析,得到如下表所示数据.
①在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为0.15mol/(L.min);n3=n4(填“>”、“<”或“=”),该反应的平衡常数的值为2.8.
②若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,则N2O4的起始浓度是0.1mol/L;假设从放入N2O4到平衡时需要80s,则达到平衡时四氧化二氮的转化率为60%.
 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.(1)电解NO制备NH4NO3,其工作原理如图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是NH3,理由是:根据反应:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3.
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3?)、c(NO2?)和c(CH3COO?)由大到小的顺序为c(NO3-)>c(NO2-)>c(CH3COO-)(已知HNO2的电离常数Ka=7.1×10-4mol/L,CH3COOH的电离常数Ka=1.7×10-5mol/L).可使溶液A和溶液B的pH相等的方法是bc.
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)100℃时,将0.400mol 的NO2气体充入2L抽空的密闭容器中,发生反应2NO2(g)?N2O4(g)△H<0.每隔一定时间就对该容器内的物质进行分析,得到如下表所示数据.
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,则N2O4的起始浓度是0.1mol/L;假设从放入N2O4到平衡时需要80s,则达到平衡时四氧化二氮的转化率为60%.
17.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | Na2O2与水反应时,1 mol Na2O2转移1 mol电子 | |
| B. | 78gNa2O2含有阴、阳离子总数是4NA | |
| C. | 1mo1•L-1的AlC13溶液中,C1-离子的数目为3 NA | |
| D. | 5.6 g铁与足量盐酸反应转移的电子数为0.3 NA |
14.已知热化学方程式:2A(g)+B(g)?2C(g)△H=-QkJ•mol-1(Q>0).下列说法正确的是( )
| A. | 相同条件下,2molA(g)和1molB(g)所具有的总能量小于2mol C(g)所具有的能量 | |
| B. | 增大压强或升高温度,该平衡都向逆反应方向移动 | |
| C. | 将2molA(g)和1molB(g)置于一密闭容器中充分反应后,放出热量为QkJ | |
| D. | 如将一定量A(g)和B(g)置于某密闭容器中充分反应放热Q kJ,则此过程中有2molA(g)被消耗 |
15.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtWuthrich 等人为此获得2002年诺贝尔化学奖.下面有关13C、15N的叙述中正确的是( )
| A. | 13C与15N有相同的中子数 | |
| B. | 13C一种同位素14C具有放射性,14C不可用于考古断代,推算出文物的年代 | |
| C. | 一个15N的质量约为2.5×10-25 kg | |
| D. | 15N的核外电子数与中子数不相同 |




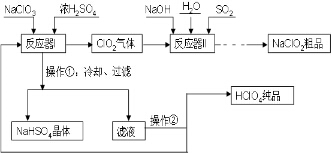 工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下: