题目内容
10.中国女药学家屠呦呦因研制新型抗疟药青蒿素和双氢青蒿素成果而获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素结构如图所示:下列关于青蒿素和双氢青蒿素的说法不正确的( )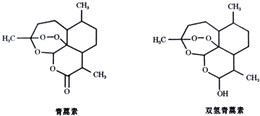
| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素和双氢青蒿素不是同分异构体 | |
| C. | 青蒿素和双氢青蒿素都能发生酯化反应 | |
| D. | 青蒿素在稀硫酸催化条件下能发生水解反应 |
分析 A.根据结构简式确定分子式;
B.青蒿素和双氢青蒿素的分子式不同;
C.青蒿素不含羟基或羧基;
D.青蒿素含有酯基,可水解.
解答 解:A.由结构简式可知青蒿素的分子式为C15H22O5,故A正确;
B.青蒿素的分子式为C15H22O5,双氢青蒿素的分子式为C15H24O5,二者分子式不同,不是同分异构体,故B正确;
C.青蒿素不含羟基或羧基,不能发生酯化反应,故C错误;
D.青蒿素含有酯基,可水解,故D正确.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
20.下列液体混合后,常温下溶液一定呈碱性的是( )
| A. | pH=8的氢氧化钠溶液1mL与999mL水混合 | |
| B. | pH=12的氢氧化钠溶液与pH=2的某酸溶液等体积混合 | |
| C. | pH=2的盐酸与0.01mol/L的氨水等体积混合 | |
| D. | 1×10-3mol/L的盐酸和4×10-4mol/L的Ba(OH)2溶液各取10mL,混合后再稀释100倍 |
1.在下列各溶液中,离子一定能大量共存的是( )
| A. | 室温下,pH=3的溶液中:AlO2-、Al3+、Cl-、SO42- | |
| B. | 含有大量Fe3+的溶液中:K+、Mg2+、S2-、NO3- | |
| C. | 由水电离的c(H+)=10-11 mol•L-1的溶液中,K+、Na+、Cl-、SO42- | |
| D. | c(H+)<c(OH-)的溶液中:Na+、NH4+、CO32-、S2- |
18.甲烷分子中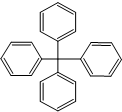 的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )
的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )
 的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )
的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )| A. | 分子式为C25H20 | B. | 所有碳原子都在同一平面上 | ||
| C. | 是共价化合物 | D. | 是纯净物 |
5.A、B、C、D为原子序数依次增大的短周期主族元素,B2-和D3+的电子层结构相同,A-的电子层结构与氦相同,C是同周期原子半径最大的元素,下列说法错误的是( )
| A. | 离子半径:B2->D3+ | |
| B. | 最高价氧化物对应的水化物碱性:C>D | |
| C. | 失电子能力:A>C | |
| D. | A与B可形成共价化合物:A2B、A2B2 |
15.某无色溶液中可能含有①Na+②Ba2+③Cl-④Br -⑤S042-⑥SO32-中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
下列结论正确的是( )
| 步驟序号 | 操作步骤 | 现 象 |
| (1) | 用pH试纸检验 | 溶液的pH>7 |
| (2) | 向溶液中滴加氯水,再加人CC14、振荡、静置 | 下层呈橙色 |
| (3) | 向(2)所得水溶液中加人Ba(N03)2溶液和 稀 HNO3 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加人AgNO3溶液和稀HNO, | 有白色沉淀产生 |
| A. | 不能确定的离子是① | B. | 不能确定的离子是②③ | ||
| C. | 肯定含有的离子是①④⑥ | D. | 肯定没有的离子是②⑤ |
19.2015年7月31日,中国获得2022年冬奥会主办权,这将促进中国冰雪运动的发展.以下关于冰的说法正确的是( )
| A. | 等质量的0℃冰与0℃的水内能相同 | B. | 冰和可燃冰都是结晶水合物 | ||
| C. | 冰和干冰、水晶的空间结构相似 | D. | 氢键影响冰晶体的体积大小 |