题目内容
已知相同条件下同浓度的NaCN与NaF的稀溶液,前者的pH值大于后者,相同条件下比较同浓度同体积两种溶液中的关系,其中正确的是( )
| A、c(CN-)>c(F-) |
| B、c(Na+)=c(CN-)=c(F-) |
| C、NaCN水解程度比NaF大 |
| D、两者所含水分子总数相等 |
考点:离子浓度大小的比较
专题:
分析:相同条件下同浓度的NaCN与NaF的稀溶液,前者的pH值大于后者,说明CN-的水解程度大于F-的水解程度,由此分析解答.
解答:
解:A.NaCN水解程度大,所以c(CN-)<c(F-),故A错误;
B、因为CN-和F-都是弱离子,要发生水解,而且CN-的水解程度大于F-的水解程度,所以c(Na+)>c(F-)>c(CN-),故B错误;
C、相同条件下同浓度的NaCN与NaF的稀溶液,前者的pH值大于后者,所以CN-的水解程度大于F-的水解程度,故C正确;
D、相同条件下比较同浓度同体积两种溶液中,NaCN水解程度大,所以水分子转化的多,即两者水分子数不等,故D错误;
故选C.
B、因为CN-和F-都是弱离子,要发生水解,而且CN-的水解程度大于F-的水解程度,所以c(Na+)>c(F-)>c(CN-),故B错误;
C、相同条件下同浓度的NaCN与NaF的稀溶液,前者的pH值大于后者,所以CN-的水解程度大于F-的水解程度,故C正确;
D、相同条件下比较同浓度同体积两种溶液中,NaCN水解程度大,所以水分子转化的多,即两者水分子数不等,故D错误;
故选C.
点评:本题考查了盐的水解,根据“含有弱根离子的盐能促进水的电离,越弱越水解PH值越大”就可分析解答本题,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学与生产、生活密切相关.下列叙述正确的是( )
| A、明矾净水和家用消毒剂的消毒原理相同 |
| B、使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| C、铝合金的广泛使用是因为人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、钒氮合金钢是“鸟巢”的主要材料之一,其熔点、硬度和强度均高于纯铁 |
下列离子反应方程式正确的是( )
| A、小苏打溶液与盐酸反应:CO32-+2H+=CO2↑+H2O |
| B、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、钠与水反应:Na+H2O=Na++OH-+H2↑ |
| D、Fe溶于稀硫酸:Fe+3H+=Fe3++H2↑ |
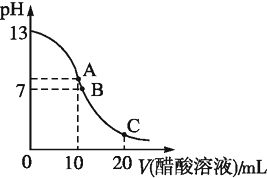 25℃时,在20mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
25℃时,在20mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )| A、在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B、在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-)) |
| C、在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D、在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
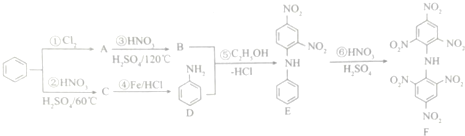
 根据化学反应原理,回答下列问题:
根据化学反应原理,回答下列问题: