题目内容
化学与生产、生活密切相关.下列叙述正确的是( )
| A、明矾净水和家用消毒剂的消毒原理相同 |
| B、使用含有氯化钠的融雪剂会加快桥梁的腐蚀 |
| C、铝合金的广泛使用是因为人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、钒氮合金钢是“鸟巢”的主要材料之一,其熔点、硬度和强度均高于纯铁 |
考点:镁、铝的重要化合物,氯、溴、碘及其化合物的综合应用,合金的概念及其重要应用
专题:化学应用
分析:A.明矾净水的原理:明矾电离产生铝离子,铝离子水解生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性,所以能净水;家用消毒液消毒的原理在水溶液中生成次氯酸,次氯酸的具有氧化作用可用于消毒;
B.原电池能加快化学反应的速率;
C.铝的冶炼通常用电解法;
D.合金熔点比其成分金属低,硬度、强度比其成分金属大.
B.原电池能加快化学反应的速率;
C.铝的冶炼通常用电解法;
D.合金熔点比其成分金属低,硬度、强度比其成分金属大.
解答:
解:A.明矾净水的原理:明矾电离产生铝离子,铝离子水解生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性,所以能净水;家用消毒液消毒的原理在水溶液中生成次氯酸,次氯酸的具有氧化作用可用于消毒,两者的原理不同,故A错误;
B.氯化钠是电解质,能与桥梁中的钢构成原电池,故B正确;
C.铝的冶炼通常用电解三氧化二铝的方法,不能用热还原法,故C错误;
D.一般来说合金熔点比其成分金属低,硬度、强度比其成分金属大,钒氮合金钢的硬度和强度均高于纯铁,但熔点低于,故D错误;
故选B.
B.氯化钠是电解质,能与桥梁中的钢构成原电池,故B正确;
C.铝的冶炼通常用电解三氧化二铝的方法,不能用热还原法,故C错误;
D.一般来说合金熔点比其成分金属低,硬度、强度比其成分金属大,钒氮合金钢的硬度和强度均高于纯铁,但熔点低于,故D错误;
故选B.
点评:本题主要考查了物质的性质与用途以及合金组成和性质分析,注意知识积累,题目较简单.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A、在有机化工中,氯气是合成塑料、橡胶、农药和人造纤维的重要原料 |
| B、汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 |
| C、白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去 |
| D、油脂是产生能量很高的营养物质,在饮食中不必控制油脂的摄入量 |
同温同压下,某气态芳香烃的密度是氢气的53倍,其中碳的质量分数为90.6%,则此烃的一氯代物有(不考虑立体异构( )
| A、13种 | B、14种 |
| C、15种 | D、16种 |
在Na2O2与CO2 的反应中,下列说法正确的是( )
| A、该反应中Na2O2 是氧化剂,CO2 是还原剂 |
| B、1mol Na2O2参加反应,有2mole-转移 |
| C、Na2O2晶体中阴阳离子个数比为1:2 |
| D、CO2分子中含有极性键和非极性键 |
下列是一些化学键的键能:
根据键能数据估算:CH4 (g)+4F2 (g)=CF4(g)+4HF(g),该反应每生成1molHF(g)( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ?mol-1) | 414 | 489 | 565 | 155 |
| A、放热485 kJ |
| B、吸热485 kJ |
| C、放热1940 kJ |
| D、吸热1940 kJ |
已知相同条件下同浓度的NaCN与NaF的稀溶液,前者的pH值大于后者,相同条件下比较同浓度同体积两种溶液中的关系,其中正确的是( )
| A、c(CN-)>c(F-) |
| B、c(Na+)=c(CN-)=c(F-) |
| C、NaCN水解程度比NaF大 |
| D、两者所含水分子总数相等 |
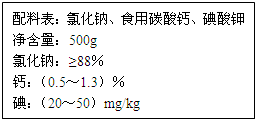 由于饮食结构和饮食习惯的影响,缺钙是国人具有普遍性的一种现象.以食盐为载体加钙,可保证人们一日三餐持续补钙.如图是某厂生产的某种加钙食盐包装标签上的部分文字,请阅读后回答以下问题:
由于饮食结构和饮食习惯的影响,缺钙是国人具有普遍性的一种现象.以食盐为载体加钙,可保证人们一日三餐持续补钙.如图是某厂生产的某种加钙食盐包装标签上的部分文字,请阅读后回答以下问题: