题目内容
16.在一定条件下,乙烷和乙烯都能制备氯乙烷(C2H5Cl).试回答:(1)上述两种制备氯乙烷的方法中,用乙烯制备氯乙烷方法好.原因是乙烷与氯气的取代反应,副反应较多,而乙烯与氯化氢的加成反应的产物是唯一的,无副产物.
(2)请写出好的制备氯乙烷(C2H5Cl)的化学方程式CH2=CH2+HCl$\stackrel{一定条件}{→}$CH3CH2Cl;该反应的类型是加成反应.
分析 乙烯与HCl发生加成反应制备氯乙烷,产物只有一种;而乙烷与氯气发生取代反应制备氯乙烷,产物复杂,以此来解答.
解答 解:乙烯与HCl发生加成反应生成氯乙烷,乙烷与氯气发生取代反应生成氯乙烷和HCl,
(1)上述两种制备氯乙烷的方法中,用乙烯制备氯乙烷方法好.原因是,
故答案为:用乙烯制备氯乙烷;乙烷与氯气的取代反应,副反应较多,而乙烯与氯化氢的加成反应的产物是唯一的,无副产物;
(2)好的制备氯乙烷(C2H5Cl)的化学方程式为CH2=CH2+HCl$\stackrel{一定条件}{→}$CH3CH2Cl,该反应为加成反应,
故答案为:CH2=CH2+HCl$\stackrel{一定条件}{→}$CH3CH2Cl;加成反应.
点评 本题考查有机物的制备实验评价,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与评价能力的考查,注意加成反应的特点及绿色化学的要求,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.在一定温度下,反应A2(气)+B2(气)?2AB(气)达到平衡状态的标志是( )
| A. | 单位时间里消耗n molA2,同时生成2n molAB | |
| B. | 容器中的总压强不随时间而变化 | |
| C. | A2、B2、AB的物质的量之比满足1:2:3 | |
| D. | 单位时间里生成2n molAB的同时生成n molB2 |
7.下列实验操作、实验现象以及实验结论完全正确的是( )
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 植物油中加入含有酚酞的NaOH溶液,微热 | 红色变浅,且不再分层 | 油脂发生了水解反应 |
| B | 柠檬醛(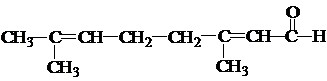 )中加入酸性高锰酸钾溶液 )中加入酸性高锰酸钾溶液 | 溶液褪色 | 柠檬醛分子中含有醛基 |
| C | 溴乙烷与NaOH溶液共热后,加入AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷发生了水解 |
| D | 向含H2SO4的淀粉水解液中加入新制的Cu(OH)2悬浊液,煮沸 | 没有砖红色沉淀 | 淀粉未水解 |
| A. | A | B. | B | C. | C | D. | D |
4.往NaOH溶液中加入少量的稀醋酸,若温度不变,下列数据一定增大的是( )
| A. | 溶液的导电性 | B. | 水的离子积 | C. | 离子总数 | D. | 溶液pH值 |
11.下列各组离子不能在指定溶液中大量共存的是( )
①加入Al能放出H2的溶液中:NH4+、SO42-、Cl-、HCO3-
②pH=13的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③水电离出来的c(H+)=10-13 mol/L的溶液:NH4+、K+、NO3-、S2O32-
④AlCl3溶液中:HCO3-、Na+、I-、HS-
⑤能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO-.
①加入Al能放出H2的溶液中:NH4+、SO42-、Cl-、HCO3-
②pH=13的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③水电离出来的c(H+)=10-13 mol/L的溶液:NH4+、K+、NO3-、S2O32-
④AlCl3溶液中:HCO3-、Na+、I-、HS-
⑤能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO-.
| A. | ①②③④ | B. | ①③④⑤ | C. | ②④⑤ | D. | ②③④⑤ |
1.已知Y元素最高正价与最低负价的绝对值之差是4,Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
| A. | KCl | B. | K2S | C. | Na2S | D. | Na2O |
 ,W与R形成的化合物的化学式为Na3N.它们的晶体属于离子晶体.
,W与R形成的化合物的化学式为Na3N.它们的晶体属于离子晶体.