题目内容
18. 某ⅡA族元素是该族元素中在自然界最广泛存在的元素,常以化合物F的形式存在,其单质A可发生一系列如图所示的化学反应.下列说法正确的是( )
某ⅡA族元素是该族元素中在自然界最广泛存在的元素,常以化合物F的形式存在,其单质A可发生一系列如图所示的化学反应.下列说法正确的是( )| A. | D与H溶液反应后所得溶液的溶质成分有三种可能 | |
| B. | 电解F与盐酸反应后的溶液以制取单质A | |
| C. | 反应①、③中消耗相同H2O时反应转移电子数相同 | |
| D. | 工业上常用F的悬浊液与Cl2反应制取漂白粉 |
分析 在自然界存在最广泛的ⅡA族元素中常温下与水反应的是单质Ca,与水反应生成Ca(OH)2和H2,则A是Ca,B是H2,C是Ca(OH)2,E是NaH,H是NaOH,CaCO3受热分解生成CO2和CaO,而CO2恰好与Ca(OH)2反应生成CaCO3和H2O,所以D和G分别是CO2和CaO,F为CaCO3,以此解答该题.
解答 解:在自然界存在最广泛的ⅡA族元素中常温下与水反应的是单质Ca,与水反应生成Ca(OH)2和H2,则A是Ca,B是H2,C是Ca(OH)2,E是NaH,H是NaOH,CaCO3受热分解生成CO2和CaO,而CO2恰好与Ca(OH)2反应生成CaCO3和H2O,所以D和G分别是CO2和CaO,F为CaCO3,
A.CO2对应的碳酸是二元酸,与NaOH反应时可能会生成两种碳酸盐:Na2CO3和NaHCO3,所得溶液的溶质成分有二种可能,故A错误;
B.Ca作为活泼的金属元素一般只能通过电解法来制备,可用电解熔融的CaCl2的方法制备,但不能用氯化钙溶液制备,因钙为活泼金属,可与水反应,故B错误.
C.反应①为Ca+2H2O═Ca(OH)2+H2↑,消耗1molH2O时,反应转移电子数为1mol,反应③为NaH+H2O═NaOH+H2↑,消耗1molH2O时,反应转移电子数为1mol,故C正确;
D.F为CaCO3,工业常用Ca(OH)2的悬浊液与Cl2反应制取漂白粉,故D错误;
故选C.
点评 本题主要考查常见金属单质及其化合物之间的相互转化,注意框图推断题的突破口,熟悉元素化合物的性质,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列说法不正确的是( )
| A. | 假说经过反复验证和修正,才发展成为科学的理论 | |
| B. | 研究物质的性质常用观察、实验、分类、比较等方法 | |
| C. | 胶体中分散质微粒能透过滤纸不能透过半透膜 | |
| D. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
9.NA表示阿伏加德罗常数,下列说法不正确的是( )
| A. | H2SO4的摩尔质量(kg/mol)与NA个硫酸分子的质量(g)在数值上相等 | |
| B. | NA个氧气分子和NA个氮气分子的质量比为8:7 | |
| C. | 1.5 L 0.3 mol•L-1Na2SO4溶液中含0.9NA个Na+ | |
| D. | 非标准状况下,22.4LO2中含有氧分子可能为NA个 |
6.5.5g某气体中含有7.525×1022个气体分子,则该气体可能为( )
| A. | CO2 | B. | CO | C. | N2 | D. | O2 |
13.化学在生产和日常生活中有着重要的作用.下列有关说法正确的是( )
| A. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 | |
| C. | 福尔马林可作食品的保鲜剂 | |
| D. | 浓硫酸可刻蚀石英制艺术品 |
10.关于实验事故或药品的处理方法中,正确的是( )
| A. | 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 | |
| B. | 制取蒸馏水时,为了防止瓶内产生暴沸现象,应先向烧瓶内加几片碎瓷片 | |
| C. | 配制稀硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 不慎洒出的酒精在桌上着火时,应立即用大量水扑灭 |
8.在[Pb2+]为0.200mol/L的溶液中,若每升加入0.201mol的Na2SO4(设条件不变),留在溶液中的Pb2+的百分率是(已知PbSO4的Ksp=1.8×10-8)( )
| A. | 1×10-3% | B. | 2×10-4% | C. | 9×10-3% | D. | 2.5×10-20% |

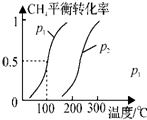 甲醇是一种重要的化工原料,在生产中有着重要的应用.工业上用天然气为原料,分为两阶段制备甲醇:
甲醇是一种重要的化工原料,在生产中有着重要的应用.工业上用天然气为原料,分为两阶段制备甲醇: